PROTAC技术在肿瘤靶向治疗新方向
来源:综合整理 | 发布时间:2023-09-25
摘要:过去十年,药物靶标领域的格局发生了重大变化。尽管传统靶标(比如激酶,G蛋白偶联受体)依然是主方向,但是目前风向也慢慢从传统药物靶标转向更具挑战性的“不可成药”靶标。
过去十年,药物靶标领域的格局发生了重大变化。尽管传统靶标(比如激酶,G蛋白偶联受体)依然是主方向,但是目前风向也慢慢从传统药物靶标转向更具挑战性的“不可成药”靶标。
近年来,研究者在药物化学探索过程中逐步开发出新的靶向蛋白,其中小分子诱导的蛋白降解技术是一个非常火热的赛道,其中就包括了发展迅速的PROTAC技术。PROTAC的概念于2001年由耶鲁大学的Craig Crews团队和加州理工大学的Deshaies团队首次提出,是靶向蛋白降解技术起步最早、研究最为成熟的系统。作为新兴治疗药物,PROTAC拓展了可成药靶标的覆盖范围、并具有克服耐药性和降低靶标关联毒性(On-target toxicity)方面表现出巨大的优势,因此在生物医药领域引起了学术界、产业界和投资界引起广泛关注,也为药物开发提供新的思路。而PROTAC技术本身不管是从技术积累还是从商业化角度来说,成熟度都更高。
本期我们就“PROTAC技术领域”的一些情况,截止至2023年9月进行了收录整理。
一、PROTAC简介
1、提出
PROTAC(Proteolysis Targeting Chimeras)是一种蛋白降解靶向联合体的概念,最早由耶鲁大学教授Craig Crews等人在2001年提出。它利用机体内天然存在的蛋白清理系统,通过降低蛋白水平而不是抑制蛋白的功能来治疗疾病。经过20年的发展,PROTAC技术已经成为当前新药研发领域最受关注的技术之一,备受科研院所、药企和投资机构的青睐。
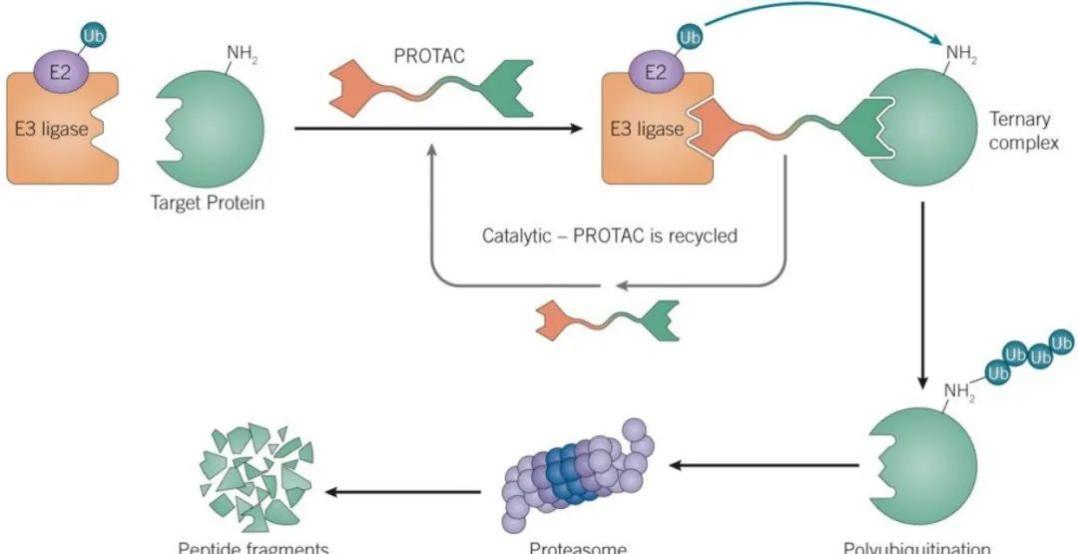
图:PROTAC作用机制
与传统小分子药物相比,基于PROTAC的蛋白降解剂具有独特的优势。其中最大的优势之一是能够靶向难以成药的靶点或突变蛋白。研究表明,目前药物开发的靶点不到20%,有高达80%的蛋白质靶点无法通过传统药物研发手段干预。此外,PROTAC分子不需要与靶蛋白长时间结合,就能降解靶蛋白使其完全消除功能,有望解决小分子抑制剂常出现的耐药性问题。
2. 作用机制
PROTAC结构包括三个部分,即一个E3泛素连接酶配体、一个靶蛋白配体和特殊设计的“Linker”结构对其进行连接。其作用机制如下图所示。
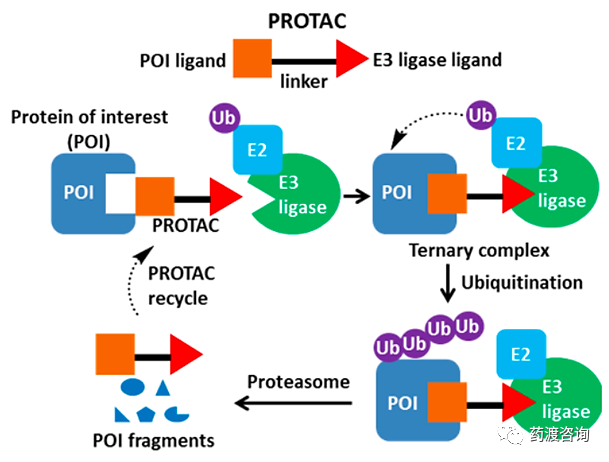
图:PROTAC结构及诱导蛋白质降解机制
数据来源:药渡咨询
3、发展历程
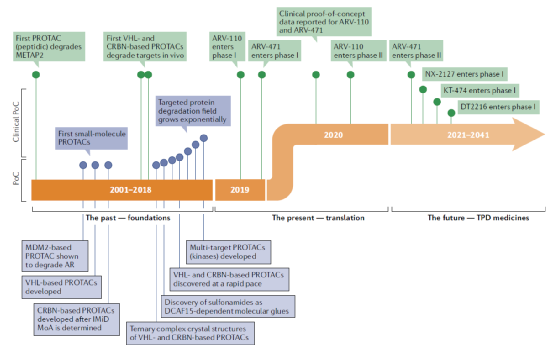
图:PROTAC发展历程
PROTAC的第一个时代始于2001年Sakamoto等人发表的关键性论文,首次在体外验证了PROTAC的概念。早期的PROTAC被称为“生物PROTAC”,因为它们不是纯粹的小分子结构,而是包含了E3连接酶的肽配体。然而,随后发现了HIF1α肽的小分子模拟物,为基于小分子结构的完全PROTAC的设计开启了新的可能性。自此以后,PROTAC领域的分子开发经历了指数级增长。
自2013年以来,Arvinas、C4 Therapeutics、Kymera Therapeutics等公司相继成立,专注于开发蛋白质降解技术。制药巨头默克、基因泰克、辉瑞、诺华、勃林格殷格翰等也纷纷进入该领域。
2019年,第一个进入临床试验的PROTAC药物ARV-110通过将雄激素受体招募到CRL4-CRBN连接酶复合物中来靶向雄激素受体,终结了靶向蛋白质降解的基础时代。从那时起,PROTAC进入了临床转化时代,设计用于降解致病蛋白质的多个分子进入临床,这一领域变得非常热门。
在PROTAC概念提出20年后,截至2021年底,至少有25家企业专注于PROTAC药物的研发,已有15种不同的靶向蛋白质降解剂进入临床试验,预计未来会有更多的临床项目推进。
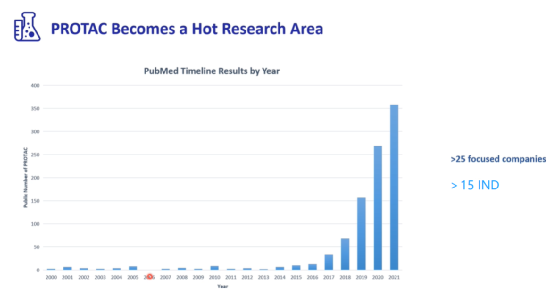
图:PROTAC药物研发(2000年—2021年)
二、PROTAC的技术优势
传统小分子抑制剂采用“占据驱动”模式,即在较高浓度时才能占据靶点的活性位点,通过阻断下游信号通路传导起到治疗疾病作用,但存在易“脱靶”且需要明确活性位点局限。PROTAC技术可直接诱导底物蛋白降解,打破“占据驱动”局限,具备以下明显优势:
1、可靶向“不成药”靶点:PROTAC只要能够产生结合作用就可以诱导相关蛋白被降解,且活性较高,可大大提高靶点的范围。
2、克服“耐药性”:传统小分子药物高亲和力的结合容易造成靶蛋白突变或过表达,即使后续迭代研发,也会产生新的耐药性。PROTAC分子通过UPS将靶蛋白降解掉,很大程度从根源上避免了耐药性问题。
3、特异性强,安全性高:相比小分子可靶向多个蛋白易引起脱靶毒性,PROTAC各部件之间协同作用,使其特异性增强。在催化剂量下,可降解靶向蛋白且自身不参与反应,蛋白降解后会自动解离进入下一循环,使得安全性提高。
4、可通过血脑屏障:血脑屏障除了允许特定类型的分子通过,PROTAC对其具有穿透能力,提示PROTAC还可用于神经及精神疾病治疗。
5、给药途径多样:PROTAC可通过静脉、口服等多种给药方式,避免了长期单一方式用药给患者带来的心理负担,提高患者依从性。除此之外,将PROTAC技术与其他治疗方案从靶点位置、给药分布、靶向支架蛋白、口服利用度、生物选择性、给药途径等方面进行对比,结果如下表所示。
表:PROTAC与其他治疗方案对比情况 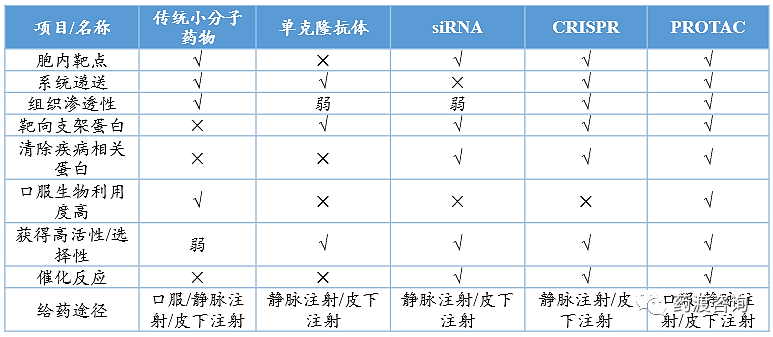
数据来源:药渡咨询
由上表可知,与传统小分子药物、单克隆抗体、siRNA和CRISPR对比,PROTAC在靶点位置、给药分布、靶向支架蛋白、口服利用度、生物选择性、给药途径等方面具有明显优势。
三、PROTAC的研发布局
1、全球研发布局
2019年,全球首个PROTAC候选药物ARV-110进入临床Ⅰ期研究阶段,拟用于治疗去势抵抗性前列腺癌(mCRPC)。目前全球范围内尚无获批上市的PROTAC药物,但进入临床开发阶段的PROTAC药物已经显示了初步的疗效。截至2023年6月28日,全球范围内进入临床开发阶段的PROTAC在研药物有28款,其中有1个处于临床Ⅲ期,7个处于临床Ⅱ期,20个处于临床Ⅰ期,研发进度较快的药物包括Arvinas公司的ARV-471、ARV-110和ARV-766等。我国也有多款药物进入临床开发阶段包括珃诺生物RNK-05047、海思科HSK-29116、百济神州的BGB-16673等。
据报道,PROTAC总计有超1000个具有潜在开发机会的靶标,包括激酶、BET家族蛋白、核受体、转录因子等,目前已经完成针对其中200多个靶标的PROTAC设计。已进入临床开发阶段的PROTAC靶标包括ER、AR、BTK、BRD9、TRK、STAT3、KRAS、EGFR、BRAF、IRAK4等,在研的适应症主要是肿瘤,还包括特应性皮炎、脱发等。
表:全球范围内临床在研的PROTAC药物
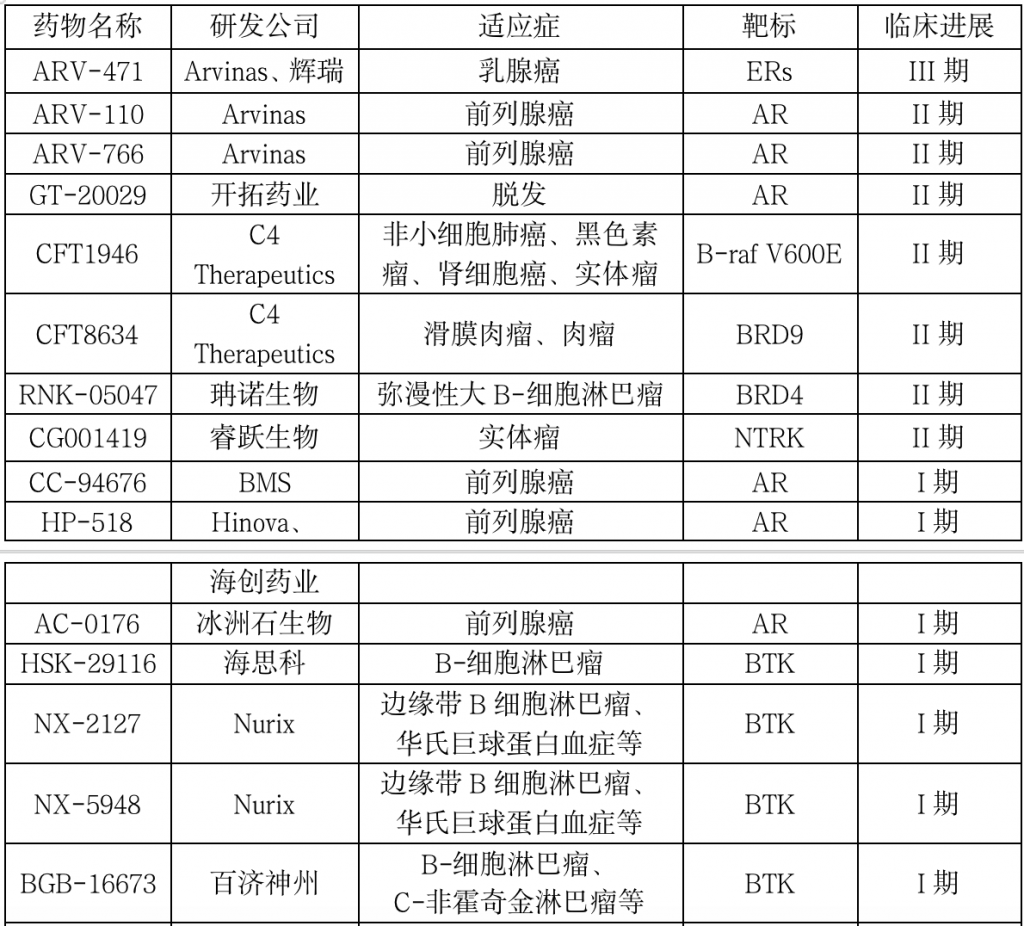
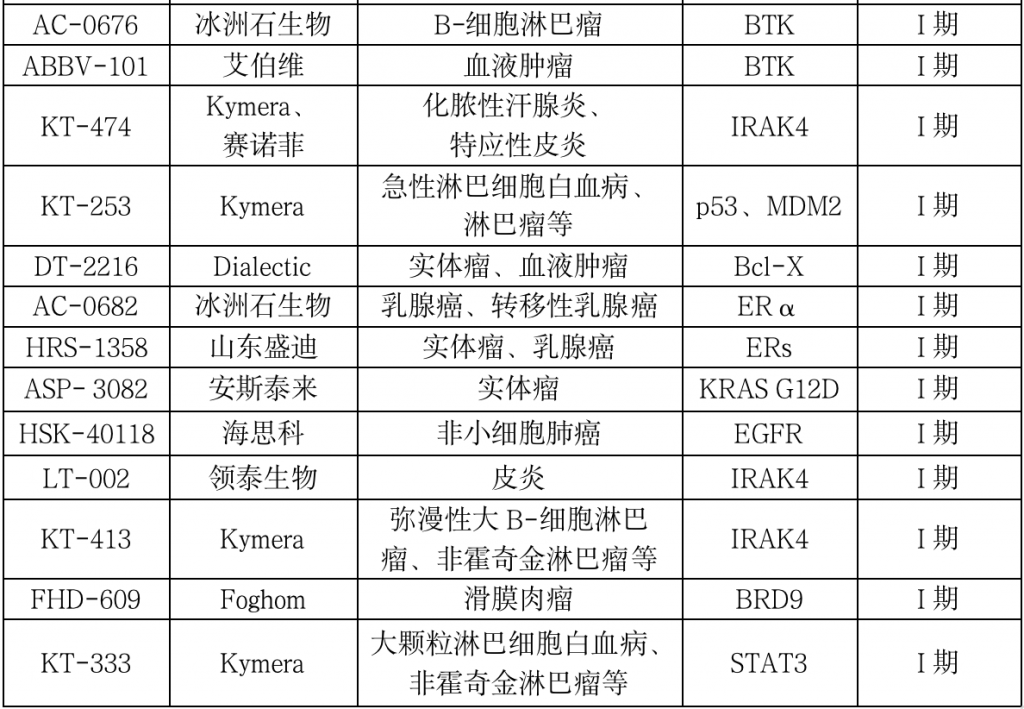
数据来源:综合整理
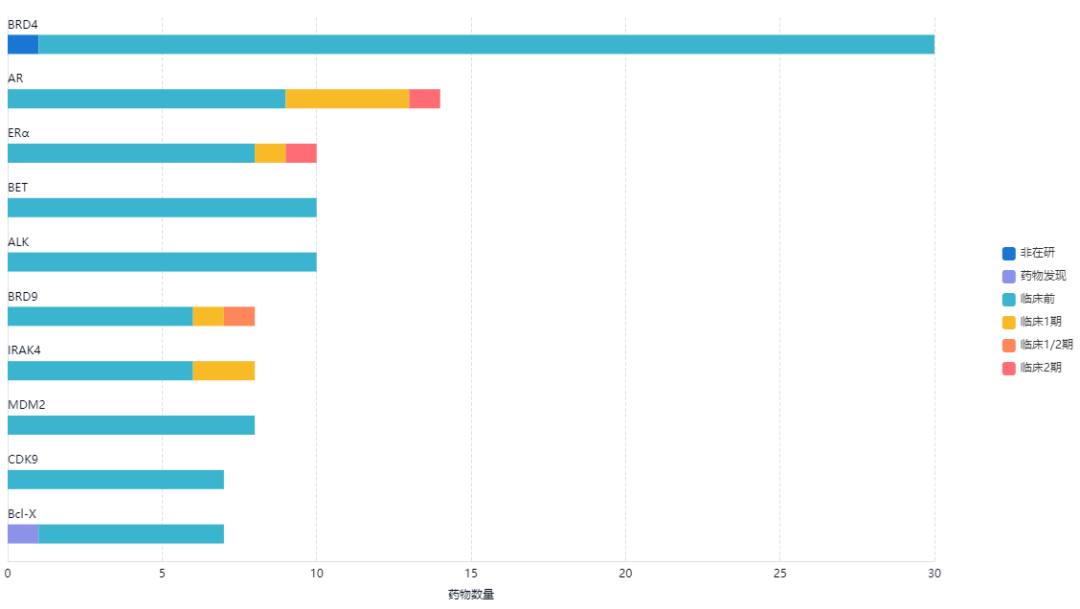
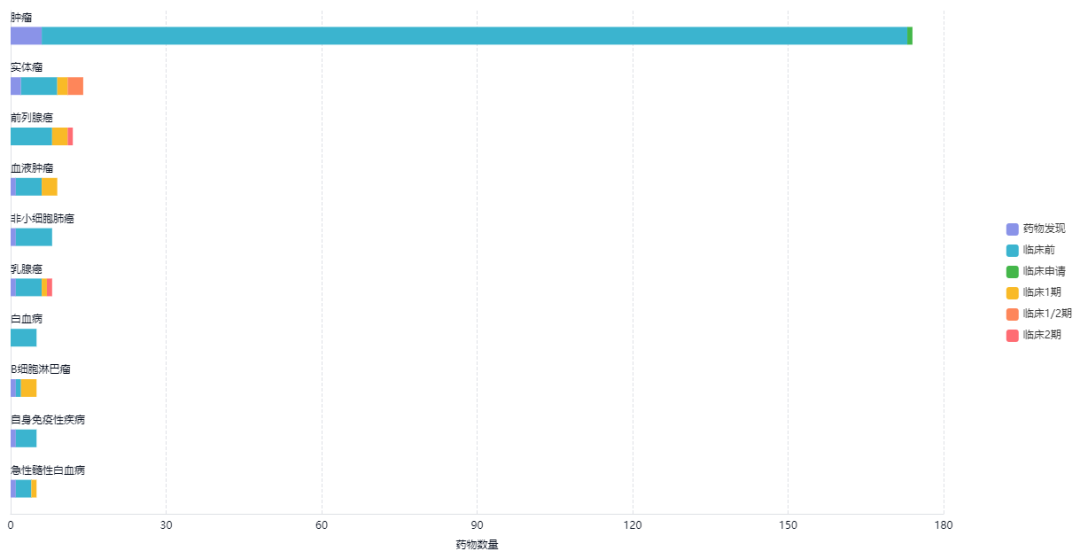
从靶点布局的情况来看,BRD4是布局最多的,但发展并不成熟,相对来讲比较成熟的靶点当属AR, ERα和BRD9。而布局的适应症多为实体瘤和血液瘤,其中前列腺癌是比较多的。
2、海外产业布局
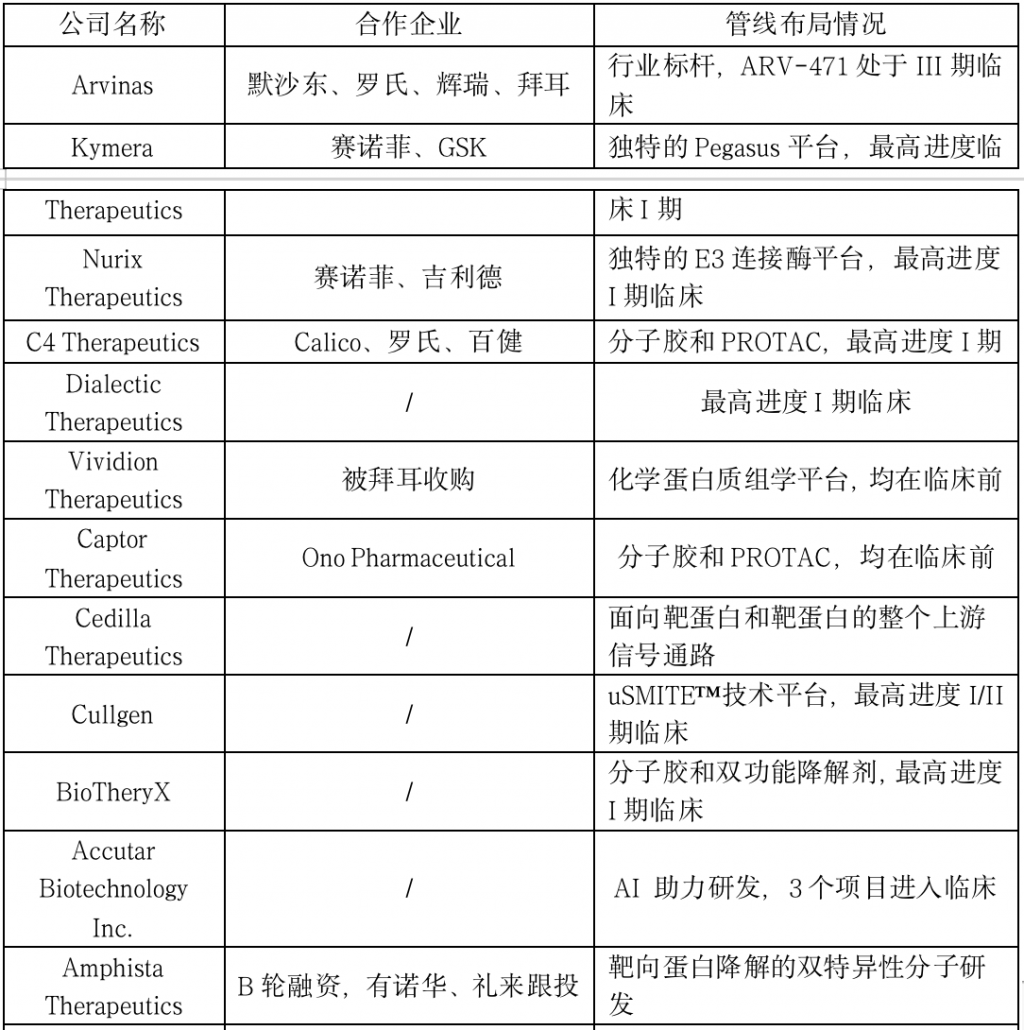
一方面,PROTAC创业公司不断涌现,例如Arvinas、Kymera Therapeutics、Nurix Therapeutics、C4 Therapeutics和Vividion Therapeutics等,这类公司大多是由PROTAC领域的研究先驱创办的,或脱胎于投资机构孵化器,或大学衍生企业。值得一提的是,近几年初创公司更多的聚焦于分子胶、LYTAC、RIPTAC等蛋白降解新技术领域;另一方面,大型制药巨头大多以和小型Bio-Tech公司频繁合作为主,例如罗氏、渤健、葛兰素史克、赛诺菲、吉利德、拜耳、辉瑞以及默沙东等知名药企已与业内公司就PROTAC技术达成相关合作。此外,一些制药巨头,例如诺华和安进等还通过招揽高端人才拓宽自主研发管线的方式进行相关布局;百时美施贵宝公司则以740亿美元收购Celgene的交易扩大了在蛋白降解领域的商业版图。
表:蛋白降解领域部分海外初创企业

3、国内产业布局
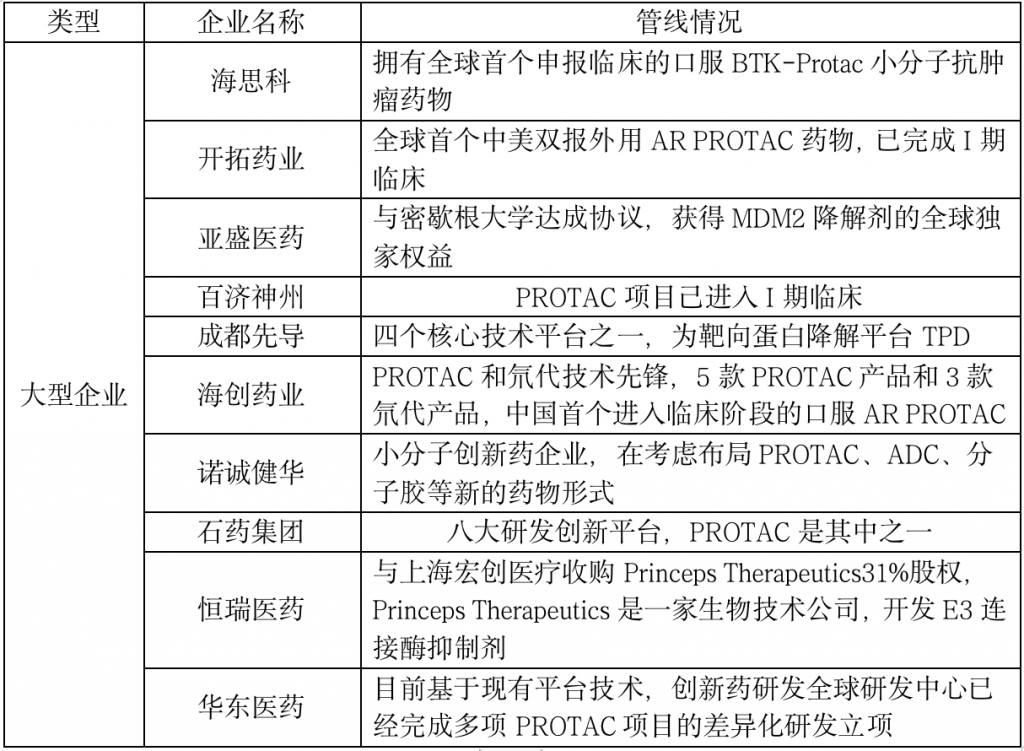
随着近几年国内医改推进及国家鼓励创新研发,专注这一新技术研发的初创公司逐渐显现,其中有不少是前国际医药巨头的相关研发负责人归国创立的,例如冰洲石医药、领泰生物、珃诺生物、多域生物、星亢原生物、分迪药业、奥瑞药业等;此外,这一赛道也吸引了国内大药企的关注,包括海思科、开拓药业、海创药业、诺诚健华、恒瑞医药、亚盛医药、石药集团、华东医药等纷纷布局该领域;同时,国内也诞生了一些提供PROTAC技术服务的平台公司,比如药明康德、美迪西等。但总体而言,国内PROTAC技术的整体研发进度大多处于早期阶段。
表:PROTAC 技术服务平台初创公司-中小企业

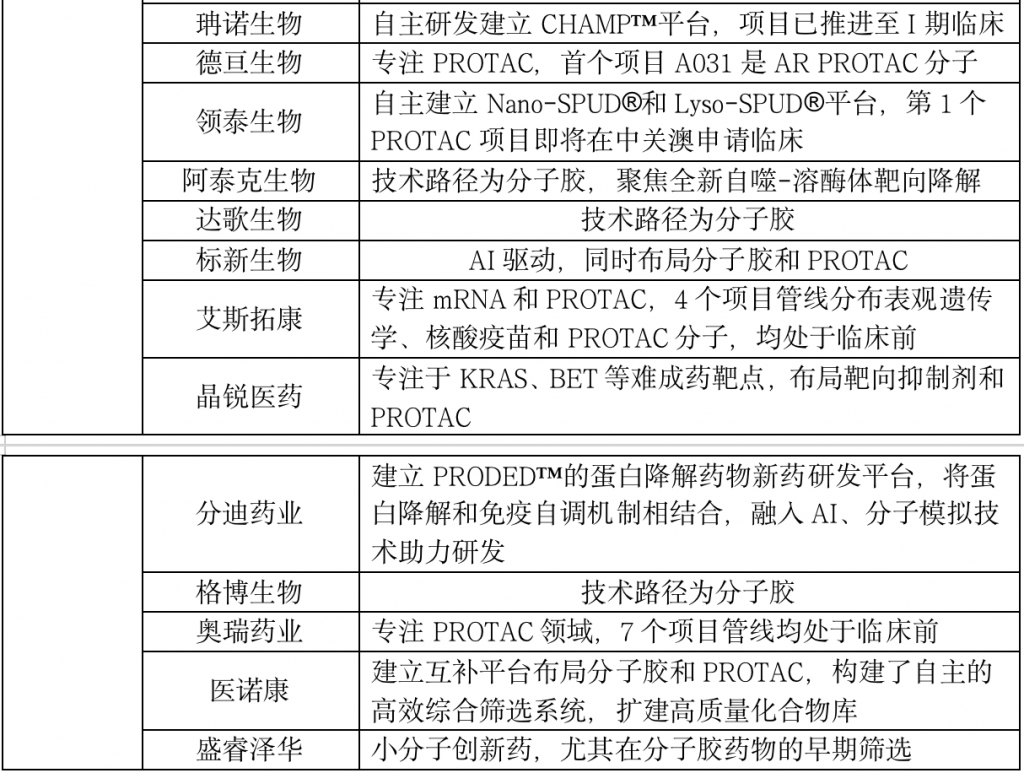
表:PROTAC 技术服务平台初创公司-大型企业
四、PROTAC发展方向及市场前景
结合PROTAC自身优势与不足,PROTAC领域的下一个里程碑将主要集中在以下四个方面:
方向一:确定最佳的蛋白降解靶点。
有报道称,最佳PROTAC靶点需满足以下原则:
①可通过过表达、突变、聚集、异构体表达或定位而偏离自然状态,产生致病性;
②E3连接酶可接近的结合表面;
③理想情况下,一个非结构化的区域可以插入蛋白酶体;
④对靶向疗法产生耐药性突变;
⑤具有支架功能;
⑥具有“不成药性”。
目前,仅1/4的人体激酶被确认用作PROTAC靶点,其中绝大多数是传统小分子抑制剂的较成熟靶点,提示小分子药物未成药的靶点开发空间较大。
方向二:扩大E3连接酶应用范围。人体基因组编码超过600种E3泛素连接酶,然而现阶段仅VHL和CRBN等少数几种用作PROTAC中的E3连接酶。未来可通过寻找广泛使用且普遍存在的连接酶,或根据连接酶的组织和细胞特异性、肿瘤富集等关键性特征不断扩大E3连接酶应用范围。
方向三:扩展临床治疗范围。蛋白降解剂的研究主要集中在肿瘤领域,考虑到蛋白降解剂应用范围广泛,能够降解任何选择目标的特点,未来可将临床治疗范围扩展至肿瘤学以外的疾病领域。目前,在神经退行性疾病、炎症、免疫学领域已初见成果。
方向四:探索PROTAC创新模式。对PROTAC创新模式的不断开发可进一步扩展PROTAC的靶点范围。如:生物制品的PROTACs(bioPROTACs)和杂合体PROTACs(hybrid PROTACs),以及创新蛋白降解模式靶向自噬体的AUTAC,自噬体牵引的ATTAC,靶向溶酶体的LYTAC和基于抗体的AbTAC等。
从PROTAC进展较快的几个靶标来看,目前已上市的BTK抑制剂、AR抑制剂、ER抑制剂和EGFR抑制剂的销售总额已超千亿元。而PROTAC针对其中耐药性靶标,对于前列腺癌、乳腺癌、淋巴瘤来说,病人生存期较长,超过半数患者能用到三线以后药物,非小细胞肺癌的患者用到三线以后药物的比例可能会低于50%。考虑到竞争者的存在,若PROTAC药物未来成功获批上市,市场空间有望达到百亿元。此外,BRD4、BRD9、IRAD4等靶标暂时没有小分子抑制剂获批上市,这些领域未来也会给PROTAC药物带来可观的市场。
五、结语
作为一种革命性技术,PROTAC已经历了20年的发展,尤其在过去5年内发展迅猛,俨然已经成为新药研发的新风口。无论是PROTAC技术领域的创业公司不断涌现,还是国际制药巨头在该领域的频繁合作,以及资本动辄上亿美元甚至高达几十亿美元的活跃市场表现,都是PROTAC技术领域研究热度的表现。
据不完全统计,全球PROTAC技术领域的融资额已超过70亿美元。虽然目前全球尚无PROTAC药物上市,但最近在I期和II期临床试验中的阳性结果,也让我们看到了PROTAC在肿瘤和其它疾病治疗中的巨大潜力。相信随着科技的发展和进步,PROTAC技术难点有望一一被攻克。
PROTAC可布局的靶点广阔,市场巨大,相信随着该技术的不断进步和完善,PROTAC可以像小分子抑制剂、单抗和免疫治疗等一样成为成功的疗法。随着技术的革新,PROTAC将会在临床上有所突破,使更多的疾病患者从中受益。
参考文献:
- 干货!PROTAC:概述,历程、原理、靶点,合联启程GMP
- PROTAC:纾困破局,续写小分子药物“人间四月”,药渡咨询
- 聚焦不可成药靶点:PROTAC风口已至,一览国内外研发格局,医麦客
- 了解PROTAC的前世今生,小药说药
- 药谷深观 | 市场表现活跃、受研究者和投资者青睐,PROTAC赛道为什么火了? 药谷君
- 华东医药官网
- 产业漫谈 | 第12期 PROTAC技术及产业进展(上篇),枫林生命健康
- 产业漫谈 | 第13期 PROTAC技术及产业进展(下篇),枫林生命健康