干细胞疗法多家新势力企业盘点及未来发展前景
人体干细胞就像是一个未接受过任何专业训练的学生,具有从事各种职业的潜能,比如修复损伤组织细胞、替代损伤细胞的功能或刺激机体自身细胞的再生功能。
在我们身体的这个社会中,每一个体细胞都被训练得高度“专业”以适应自己的功能,但干细胞还像是一个未接受过任何专业训练的学生,具有从事各种职业的潜能,比如修复损伤组织细胞、替代损伤细胞的功能或刺激机体自身细胞的再生功能。而这恰恰是干细胞的迷人之处。因而,干细胞研究在全世界范围内都处于遍地开花的状况。
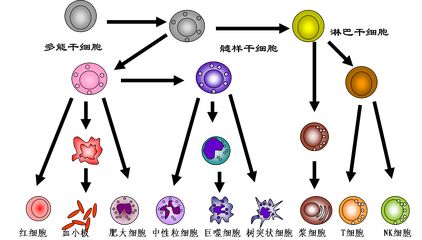
干细胞是没有经过分化的细胞,也就是没有特殊功能的细胞。皮肤细胞可以保护身体,肌肉细胞可以收缩,神经细胞可以传递讯息;干细胞却没有任何特殊结构或功能,但干细胞有种潜力,就是变成人体中任何一种细胞。
事实上有很多种干细胞,都可以为科学家所用,应用在医疗或研究上。
按照发育阶段分类,可分为胚胎干细胞(Embryonic Stem Cell)和成体干细胞(Adult Stem Cell)。
胚胎干细胞包括ES细胞(Embryonic Stem Cell)、EG 细胞(Embryonic Germ Cell)。
成体干细胞包括神经干细胞(Neural Stem Cell,NSC)、血液干细胞(Hematopoietic Stem Cell,HSC)、骨髓间充质干细胞(Mesen chymal Stem Cell,MSC)、表皮干细胞(EPidexmis Stem Cell)等。
按分化潜能,干细胞可分为,全能干细胞,多能干细胞,单能干细胞。
全能干细胞:具有形成完整个体的分化潜能,如受精卵。
多能干细胞:具有分化出多种细胞组织的潜能。如胚胎干细胞(ES)。
单能干细胞:只能向一种或两种密切相关的细胞类型分化。如神经干细胞、造血干细胞。
一、干细胞应用领域
如今,全球干细胞治疗市场已经涌现了大量的新研究、新项目以及新疗法,其中大多数疗法处在研发管线中,少数已经获得了监管机构批准上市。
统计发现,间充质干细胞的临床试验涉及上百种疾病。神经系统、心血管和骨科疾病是三类主要的研究领域,占比都在15%以上,总和超过一半。另外,糖尿病、GVHD的比例都在5%左右,是间充质干细胞临床应用的重要研究方向。
具体而言,脊髓损伤、多发性硬化、中风、肌萎缩侧索硬化症、老年痴呆症、骨关节炎、股骨头坏死、椎间盘退化、心肌梗死、肝硬化、克罗恩病、间质性肺病、系统性红斑狼疮、勃起功能障碍以及卵巢早衰是研究得较为多的疾病。未来这些患者有望更早地受益于间充质干细胞治疗。
图:干细胞技术临床应用
目前,国际上已经有间充质干细胞治疗产品获批上市。根据统计,全球已有超过13项干细胞治疗药物上市,其中绝大多数都属于间充质干细胞产品。随着临床试验的开展,未来会有更多的间充质干细胞治疗产品获批上市,受益的患者也将更多。
二、干细胞发展史
1878:出现第一篇哺乳类的体外受精卵报导。
1959:完成第一例兔子的体外受精卵。
1960:展开畸胚瘤的研究。
1968:爱得华(R.G. Edwards)和贝敏思特(B.D. Bavister)进行人类的体外受精研究。
1970:利用畸胚瘤细胞注入老鼠胚胎,制造镶嵌鼠以进行胚胎发育的研究。
1978:世界第一个试管宝宝路易丝.布朗(Louise Brown)在英国诞生。
1980:肯蒂丝.瑞得(Candace Reed)成为澳洲的第一个试管宝宝。
1981:艾凡斯等(M.J. Evans, et al.)体外培养老鼠的胚胎干细胞;伊莉莎白.卡尔 (Elizabeth Carr)成为美国的第一个试管宝宝。
1984~1988:安德鲁等(P.W. Andrews, et al.)在体外培养人类畸胚瘤细胞。
1989:佩拉等(M.F. Pera, et al.)制造人类畸胚瘤细胞株。
1994:首次使用人类人工受精的囊胚进行干细胞的研究。
1995~1996:从恒河猴取得胚胎干细胞,并在体外培养分化成三种胚层。
1998:詹姆士.汤姆生(James Thomson)从人类体外受精卵取得胚胎干细胞,并 能稳定地在体外培养;吉尔哈特(J. Gearhart)从妊娠中止的胎儿内取出其卵巢或睪丸组织, 得到一种具有干细胞特性的原始生殖细胞,称为人类生殖干细胞。
1999:《科学》(Science)杂志公布干细胞为世界十大科技进展榜首。从小鼠肌肉组织取得的成体干细胞可以「横向分化为血液细胞」。此后,科学家相继证实成体干细胞具有可塑性。
2000:美国61名诺贝尔奖得主及其它科学家联名要求美国政府对干细胞研究给予全面支持,同年美国总统柯林顿宣布美国政府准许用政府经费进行人体胚胎干细胞研究。
2001:胚胎干细胞株可以培养出神经、胰岛等更多种类的细胞。美国总统布什宣布联邦政府将优先资助胚胎干细胞研究。
2002:《自然》(Nature)杂志评选「干细胞的争议」为二○○二年科学界年度重大新闻。
2011:克隆制造干细胞被时代杂志评为2011年十大医学突破之一。
2012:诺贝尔生理医学奖授予干细胞研究科学家。
三、干细胞研发方向
1、抵抗衰老
随着现代科学技术的发展,尤其是干细胞研究的不断深入,通过补充外源干细胞抗衰老,是目前最为有效的抗衰老治疗手段。美国《科学》杂志将干细胞的研究成果列在十大科学进展的首位。干细胞抗衰老是再生医学中最核心的医疗技术,它最显著的作用就是补充种子细胞替代衰老细胞。
干细胞技术是再生医学中最核心的医疗技术,它好比我们身体的某个器官组织受损之后能使其自我再生的细胞,形象地说就像壁虎断了尾巴之后能再生同一个原理。
通过对干细胞进行分离、体外培养、定向诱导、甚至基因修饰等过程,在体外繁育出全新的、正常的甚至更年轻的细胞,并最终通过细胞组织或器官的移植实现对临床疾病的治疗和抗衰老的目的。
2、肝硬化
在肝纤维化特别是肝硬化时,因过量纤维结缔组织增生挤压,正常功能的肝细胞数量大为减少。
干细胞在肝损伤环境中可以分泌不同水平的细胞因子,表现出抗纤维化、抗炎症反应的作用,刺激肝脏产生新的肝细胞。
主要指标:
患者临床症状(乏力、纳差、腹胀等)的改善情况及不良反应的发生,检测术前及术后肝功能指标:谷丙转氨酶,白蛋白,总胆红素等的水平及腹水变化。
症状改善:
临床研究结果显示,多数患者接受自体骨髓干细胞后临床症状评分比治疗前明显改善,丙谷转氨酶(ALT)、总胆红素(TBIL)逐级降低,血清白蛋白(ALB)、胆碱酯酶(CHE)逐渐升高,特别是远期可以显著提高肝脏合成白蛋白的能力,提示患者肝功能明显改善。总有效率约80%以上。
安全性与适应症
安全性:采用自体骨髓的干细胞进行移植可以完全克服免疫排斥问题。患者移植术中和术后,无明显不良反应和并发症发生。干细胞移植治疗失代偿期肝硬化是一种较安全的治疗方法,可起到暂时性的肝脏支持作用。
适应症:中毒性、炎症性、慢性损伤性肝脏疾病,早中期肝硬化,难治性低蛋白血症(难治性腹水),反复发作黄疸等患者。
3、风湿病
MSCs(间充质干细胞)能够抑制淋巴细胞的自身免疫反应,减少促炎细胞因子的分泌,增加抗炎细胞因子的分泌。因此,推测MSC可通过免疫调节的方式阻断RA的发病,且间充质干细胞治疗对人体各项指标无明显改变,安全性很好,为临床治疗(类风湿性关节炎)RA,寻找到一条新途径。
患者在饮食、睡眠、体力、疲劳等方面均有明显改善,全部患者满足ARA20标准,多关节疼痛、肿胀、压痛明显缓解,疼痛、肿胀的关节数减少,关节活动度增加等,且患者均无不适应症状。
4、不孕症
通过将间充质干细胞附着在可降解的智能胶原支架材料上,结合宫腔镜技术分离宫腔粘连后,将支架材料和间充质干细胞的复合体移植到宫腔内,使间充质干细胞的覆盖子宫内膜粘连面,促进了子宫内膜血管组织的再生,实现了受损子宫内膜的功能性修复。
让不能生育的妈妈获得生儿育女的能力,为久治不愈患者带来了巨大希望。
近年来,全球各界进一步开展了干细胞治疗的临床研究。美国、英国、日本等发达国家率先用干细胞移植治疗疾病的方法,并取得了不错的疗效。在我国,也有多所医院开展了间充质干细胞治疗疾病的临床研究。应用干细胞技术疗法,可以说是很多传统方法无可比拟的。
据相关数据显示,全球6000多项在研干细胞临床试验涉及上百种疾病,包括脊髓损伤、多发性硬化、中风、肌萎缩侧索硬化症、老年痴呆症、骨关节炎、股骨头坏死、椎间盘退化、心肌梗死、肝硬化、克罗恩病、间质性肺病、系统性红斑狼疮、勃起功能障碍以及卵巢早衰等等。
随着技术的不断发展,干细胞必将引发一场医疗变革,成为继药物、手术后的第三种治疗方式,各类疾病等一系列传统手段难以治疗的疑难杂症终将被逐步得到救助。
四、多家干细胞疗法企业盘点
Allele生物
发展目标——不断推进基于iPSC的细胞治疗的临床开发
成立于1999年的Allele生物专注开发临床和治疗用途的前沿技术,包括RNA干扰、荧光蛋白、诱导多能干细胞(iPSCs)、基因组编辑和单域抗体。
Aspen Neuroscience
发展目标——使干细胞治疗广泛作用于神经系统疾病
成立于2018年的Aspen Neuroscience围绕自体诱导多能干细胞(iPSC)分化多巴胺能神经元展开各项研究,目前拟提交IND,可针对性治疗散发性帕金森病。
BlueRock /Bayer
发展目标——开发神经病学、心脏病学和免疫学领域的工程细胞疗法
成立于2016年的BlueRock /Bayer移植专注于利用专有的诱导性多能干细(iPSC)平台,发掘神经病学、心脏病学和免疫学领域的治愈能量。目前,其下辖的临床1期(NCT04802733)已展开对晚期帕金森氏病的治疗。2021年,该公司于富士细胞和Opsis治疗公司建立了研发联盟,开发异基因ipsc衍生的眼病细胞疗法。
Bone Therapeutics
发展目标——应用于微创手术
该公司致力于将未分化的干细胞转化为“成骨细胞”,这些细胞可以通过微创手术使用,避免侵入性手术给患者造成更大创口。
BTX
发展目标——通过对干细胞的重新编码,作用于部分癌症
作为一家正处于临床阶段的生物制药公司,BTX注重用合成mRNA、细胞重编程、基因编辑、细胞因子开发等多种方法,完成基因编辑的iMSC和体内基因编辑。目前,旗下细胞因子药物IRX-2,正在进行2B期临床研究,适应症头颈部鳞癌。
细胞技术应用/制造领域
Cellino Biotech
发展目标——可实现个性化细胞的大规模制造
该公司善于使用机器学习、人工智能和激光技术来使细胞治疗制造变得自动化。
Exacis Biotherapeutics
发展目标——降低治疗成本,让癌症细胞治疗大众化
Exacis生物疗法公司通过采用高效的制造工艺(mRNA编辑iPSC,生产肿瘤学的工程NK和T细胞)来降低治疗成本,同时提高细胞治疗的安全性,使癌症细胞治疗大众化。
Hopstem
发展目标——同时满足多种细胞产品生产和检验所需
霍德生物以iPSCs技术为核心,进行再生医学开发。天使轮获得1200万融资,后经过5轮,获得数亿元融资。公司的核心技术之一为自主研发的RONA 2.0神经分化技术。其二期GMP生产基地位于“中国最佳医疗健康产业园区Top10”的杭州医药港,满足美国FDA及欧盟/中国cGMP要求,三套完全独立B+A和C+隔离器的无菌生产条件细胞培养间,同时满足三种不同细胞产品独立生产和检验的需求。
从时间上,我国干细胞治疗行业起步较晚,但截至2022年底,我国已经有133家研究机构通过了干细胞临床研究机构的备案,备案项目达100个;研究细分包括脐带间充质干细胞、胎盘间充质干细胞、脐带血巨核系足细胞等十二个大类,横跨神经系统、呼吸系统、皮肤、消化系统、内分泌系统等二十多个领域。
据悉,我国干细胞医疗市场的规模已经由2016年占据全球市场规模的18.6%上涨至2020年的22.1%,2020年中国干细胞医疗市场规模约为140.2亿元,而2022年市场规模将接近190.0亿元。
目前,我国已经建成完整的干细胞产业链条,即上游——干细胞提取和存储及相关设备的研发;中游——药物、再生医学产品、医美产品等研发生产单位的确立;下游——临床治疗应用。而赛桥生物、百因诺、康晟生物、金仪盛世、深研生物、中博瑞康、倍谙基生物、奥浦迈、赛动制造等,都是其中佼佼者。

五、我国干细胞疗法相关政策
行业的发展离不开政策的保驾护航。现阶段我国已明确干细胞按药品、技术管理的“双轨制”监管。企业主导研制细胞制剂鼓励按药品申报,由国家药品监督管理局(NMPA)按照药品进行监管,企业开展临床试验需要按照药物临床试验相关要求提交申请。2021年,“干细胞研究与器官修复”再被科技部列为“十四五”国家重点研发计划之中。
2022年5月10日,国家发改委正式印发了《“十四五”生物经济发展规划》,提出开展前沿生物技术创新,包括发展基因诊疗、干细胞治疗、免疫细胞治疗等新技术,强化“产学研用”协同联动,加快相关技术产品转化和临床应用,推动形成再生医学和精准医学治疗新模式,以期站在更高格局助力国产细胞技术行业释放活力。
六、干细胞治疗行业的发展前景
欧美发达国家生物技术和干细胞治疗研究起步较早,其技术相对领先,在该行业已有相对优势,位于行业顶端。我国医药产业持续稳定增长,肿瘤细胞治疗行业市场潜力巨大。自国内开展干细胞治疗项目以来,国家陆续制定相关政策扶植、医疗机构和肿瘤生物治疗企业,加大技术投入,逐步推动国内干细胞治疗市场的发展。
中国干细胞治疗技术行业的市场规模正在迅速增长,未来的发展趋势也充满希望。根据市场调研在线网发布的2023-2029年中国干细胞治疗技术行业现状分析及投资风险预测报告分析,截止至2020年,中国干细胞治疗技术市场规模已经达到500亿元,其中,干细胞治疗技术市场规模已达到330亿元。
随着科技的不断发展,中国干细胞治疗技术行业的发展将会更加迅速和蓬勃。预计,到2023年,中国干细胞治疗技术市场规模将达到1000亿元,其中,干细胞治疗技术市场规模将超过500亿元。
除此之外,在未来几年,随着技术的进一步发展,中国干细胞治疗技术行业将会有更多的创新,更多的新药和技术将会面世,这将会大大提升中国干细胞治疗技术行业的发展。
此外,随着政府加大对研发投入,中国干细胞治疗技术行业将会得到更多政府支持,这将会有助于中国干细胞治疗技术行业的发展。
总之,中国干细胞治疗技术行业的市场规模正在迅速增长,未来的发展趋势也充满希望。随着科技的不断发展,中国干细胞治疗技术行业将会更加迅速和蓬勃,更多的新药和技术也将会面世,而政府的支持也将会有助于中国干细胞治疗技术行业的发展。
未来,全球范围将有更多的干细胞药物获批上市,冲破传统治疗方法的局限性,造福人类。