未来五年有望成为重磅的11款新药!涉及基因治疗、抗体药物等领域
来源:科睿唯安 | 发布时间:2025-02-17
摘要:科睿唯安发布了一年一度《最值得关注的药物预测》报告,该报告聚焦于有望在未来五年内取得重大商业成功或革新治疗模式的11款药物。预计到2030年,这些药物将成为“重磅炸弹”药物或者能够显著提升全球患者群体的治疗效果。
科睿唯安发布了一年一度《最值得关注的药物预测》报告,该报告聚焦于有望在未来五年内取得重大商业成功或革新治疗模式的11款药物。预计到2030年,这些药物将成为“重磅炸弹”药物或者能够显著提升全球患者群体的治疗效果。本文总结了这11款药物的基本信息,供大家参考。
1、Awiqli(insulin icodec)
Awiqli是由诺和诺德公司开发的一种创新的基础胰岛素周制剂,用于治疗成人1型和2型糖尿病。
它通过提供一周一次的长效胰岛素注射,帮助患者维持全天候的血糖控制,从而简化了糖尿病管理过程。Awiqli的独特之处在于其缓释技术。它通过一种特殊的微球载体系统(基于聚乳酸-羟基乙酸共聚物 [PLGA]),将胰岛素包裹在微球中。这些微球在皮下注射后逐渐降解,缓慢释放胰岛素,旨在实现持久而稳定的胰岛素释放,以降低血糖水平,并且与每日注射的胰岛素相比,其低血糖风险较低。临床试验数据来自ONWARDS项目,这个包含6个3a期全球临床试验的大型研究项目,在超过4000名成年糖尿病患者中验证了依柯胰岛素的疗效和安全性。研究表明,相较于传统的每日基础胰岛素疗法,Awiqli能够提供相似甚至更好的血糖控制效果,同时减少了患者的用药频率,有助于提高患者的生活质量和药物依从性。欧洲药品管理局已于去年批准了Awiqli上市,这标志着全球首个每周一次的基础胰岛素制剂的诞生。
2、CagriSema(卡格列肽 + 司美格鲁肽)
CagriSema是由诺和诺德研发的一种新型复方制剂,旨在用于治疗肥胖症及2型糖尿病。
它结合了两种活性成分:长效Amylin(胰淀素)类似物Cagrilintide和长效GLP-1(胰高血糖素样肽-1)受体激动剂司美格鲁肽(Semaglutide)。这种组合通过模拟两种不同的肠道激素作用,帮助患者减轻体重并改善血糖控制。临床数据显示,在II期试验中,CagriSema表现出显著的减重效果,患者平均体重减轻达到15.6%,且超过一半的患者体重减轻≥15%;同时,HbA1c水平较基线降低了2.18%,显示出优越的降糖效果。在III期临床试验中,CagriSema与礼来公司的替尔泊肽进行了头对头比较,进一步验证其疗效。最新的数据表明,在坚持治疗的情况下,CagriSema能够使患者在68周内实现22.7%的体重减少,这比单独使用Cagrilintide或司美格鲁肽的效果更为显著,并显示出了潜在的最佳减肥疗效,有望成为市场上减重效果最为显著的药物之一。然而,这些积极的结果也伴随着市场预期的调整,当公布的数据不及最初预期时,曾导致诺和诺德股价出现波动。尽管如此,CagriSema仍然是诺和诺德未来产品线中的重要一环,具有改变肥胖症治疗格局的潜力。
3、Cobenfy(xanomeline-trospium)
Cobenfy是由Karuna Therapeutics公司开发的一种创新口服药物,旨在用于治疗精神分裂症和阿尔茨海默病引起的幻觉和妄想等精神病性症状(2023年,百时美施贵宝以140亿美元完成对Karuna Therapeutics的收购,从而获得了这款新药)。

Cobenfy的独特之处在于其采用了xanomeline与trospium的组合配方,其中xanomeline是一种选择性的胆碱能受体激动剂,能够靶向作用于中枢神经系统的毒蕈碱型乙酰胆碱受体(mAChRs),而trospium则作为一种外周抗胆碱能药物,帮助减轻xanomeline可能引发的副作用,如口干、便秘等。临床试验数据表明,在治疗精神分裂症的关键III期临床试验中,Cobenfy显示出了显著的疗效,患者在阳性和阴性症状量表(PANSS)上的得分有明显的改善,相比安慰剂组,Cobenfy治疗组的症状减少了约10分,且耐受性良好。此外,早期针对阿尔茨海默病患者的II期临床试验也显示出积极的结果,为这种新疗法在多种疾病中的应用提供了有力的支持。这些发现标志着Cobenfy有望成为一种新的、有效且耐受性良好的治疗选项,为患有相关精神健康问题的患者带来希望。
4、Ebglyss(lebrikizumab)
Ebglyss由礼来与Almirall公司共同开发,用于治疗特应性皮炎。作为一种抗IL-13抗体,Ebglyss因其较少的用药频率和强效的安全数据,有望成为中重度特应性皮炎的一线治疗选择。
Ebglyss通过特异性结合并抑制白细胞介素-13(IL-13,一种在特应性皮炎病理过程中起关键作用的细胞因子),从而减少炎症反应和改善皮肤症状。临床试验数据表明,在多项III期临床研究中,接受lebrikizumab治疗的患者显示出显著的疗效,许多患者的皮肤状况得到了明显改善,瘙痒感大幅减轻,并且生活质量有所提升。例如,在ADvocate 1和ADvocate 2这两项关键III期研究中,使用lebrikizumab治疗16周后,与安慰剂相比,达到了主要终点,即显著更多的患者实现了湿疹面积及严重程度指数(EASI)75的改善。此外,lebrikizumab的安全性和耐受性良好,为其作为治疗中重度特应性皮炎的有效新选择提供了坚实的基础。这些积极的结果使得Ebglyss成为特应性皮炎治疗领域的一个重要进展,为患者带来了新的希望。
5、Fitusiran
Fitusiran由Alnylam Pharmaceuticals和赛诺菲合作开发,用于治疗A型和B型血友病。
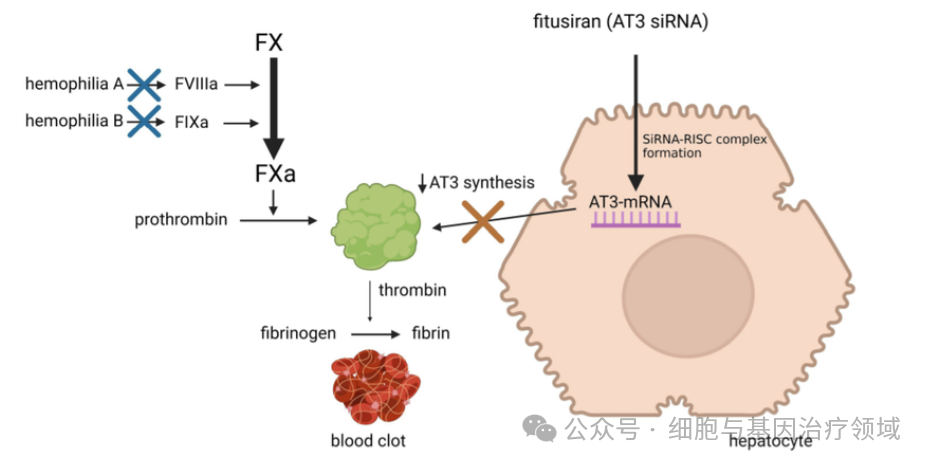
Fitusiran是一款小干扰RNA(siRNA)药物,通过靶向抗凝血酶(antithrombin, AT)的合成来增加凝血酶的生成,从而恢复凝血平衡,减少出血事件的发生。Fitusiran通过每月一次的皮下注射给药,旨在简化血友病患者的治疗管理。临床试验数据显示,在已完成的III期临床研究中,接受Fitusiran治疗的患者显示出显著减少的年出血率(ABR),并且在预防和控制出血方面表现出良好的效果。例如,在ATLAS-INH研究中,患有A型或B型血友病且具有抑制物的患者,经过Fitusiran治疗后,年出血率显著降低,多数患者的出血情况得到了有效控制。此外,Fitusiran还展示了较好的安全性和耐受性,使得其成为血友病治疗领域的一个重要进展,为患者提供了一种新的、有效的治疗选择。这一疗法不仅有望改善患者的出血症状,还能提高他们的生活质量。
6、GSK-3536819(MenABCWY)
GSK-3536819是一款由葛兰素史克(GSK)开发的五合一脑膜炎球菌疫苗,旨在预防导致大多数侵袭性脑膜炎球菌病例的五种脑膜炎奈瑟菌群。

该疫苗结合了现有MenACWY疫苗和MenB疫苗的成分,通过刺激免疫系统产生针对A、B、C、W和Y这五种血清群脑膜炎奈瑟菌的抗体,从而提供广泛的保护。临床试验数据显示,在III期临床研究中,接种MenABCWY的青少年和年轻成人参与者对所有五个血清群均产生了强烈的免疫反应,显示出高效的抗体应答率,并且安全性良好,副作用轻微且短暂,主要包括注射部位疼痛、红肿以及发热等常见疫苗接种反应。与单独接种现有的MenACWY和MenB疫苗相比,MenABCWY不仅简化了接种程序,减少了接种次数,同时提供了同等甚至更优的保护效果。这一新型疫苗的推出极大地提升了公众对多种脑膜炎球菌血清群的防护能力,为预防侵袭性脑膜炎球菌病提供了更加便捷和全面的选择。
7、Imdelltra(tarlatamab-dlle)
由安进(Amgen)开发的Imdelltra是首款获批上市针对广泛期小细胞肺癌(SCLC)的免疫疗法。
Imdelltra是一款双特异性抗体药物。该药物通过同时结合肿瘤细胞表面的delta样配体3(DLL3)和T细胞表面的CD3,有效地将T细胞重定向至肿瘤细胞,促进T细胞对表达DLL3的肿瘤细胞进行杀伤,从而达到治疗效果。临床试验数据显示,在针对复发性小细胞肺癌患者的II期临床研究中,Imdelltra表现出显著的抗肿瘤活性,客观缓解率(ORR)达到了约40%,并且部分患者显示出持久的响应。此外,尽管存在一些可管理的副作用,如细胞因子释放综合征(CRS)和神经系统毒性,但总体上该药物的安全性和耐受性良好。这些积极的结果表明,Imdelltra为那些传统治疗方法无效或难治的小细胞肺癌患者提供了一种新的、有效的治疗选择,有望改善患者的生存期和生活质量。这一突破性的疗法标志着在攻克难治性癌症方面迈出了重要一步。
8、mRESVIA(mRNA-1345)
mRESVIA由Moderna开发,是一款基于mRNA技术的疫苗,主要用于预防呼吸道合胞病毒(RSV)引起的疾病,适用于60岁及以上的成人。

该疫苗通过传递编码RSV融合蛋白(F蛋白)的mRNA,促使人体细胞产生这种蛋白质,从而激发免疫系统生成针对RSV的抗体和T细胞反应,提供保护作用。临床试验数据显示,在III期临床研究中,mRESVIA在老年人群体中表现出显著的保护效果,疫苗效力达到了约80%以上,有效减少了由RSV引起的下呼吸道疾病的发生率。此外,该疫苗的安全性和耐受性良好,常见的副作用包括注射部位疼痛、疲劳和头痛等轻微症状。这些积极的结果表明,mRESVIA为预防RSV感染提供了强有力的手段,特别是在高风险人群中,有望大幅降低因RSV导致的严重健康问题和住院率。这一创新的mRNA疫苗标志着在对抗RSV方面取得了重要进展,为全球公共卫生带来了新的希望。
9、SEL-212
SEL-212由Sobi和Selecta Biosciences联合开发,用于治疗慢性难治性痛风及其相关的炎症症状。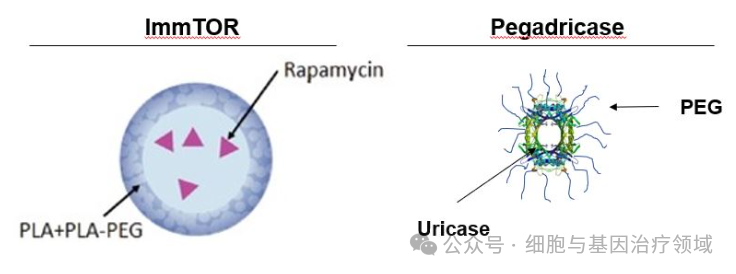
SEL-212结合了两种主要成分ImmTOR和pegadricaseSEL-212是一种创新生物制剂,其独特之处在于它结合了两种成分:pegadricase(一种经过聚乙二醇修饰的尿酸氧化酶)和ImmTOR(一种免疫调节纳米颗粒),前者能够有效降解尿酸,减少体内尿酸水平,后者则通过抑制免疫系统对pegadricase产生的抗药物抗体反应,提高治疗的安全性和持久性。临床试验数据显示,在II期和III期临床研究中,接受SEL-212治疗的患者显示出显著降低的血清尿酸水平,许多患者的痛风发作频率大幅减少,并且在维持低尿酸水平方面表现出良好的效果。例如,在一项关键的III期临床试验中,与安慰剂相比,使用SEL-212的患者达到了更高的持续尿酸控制率,同时耐受性良好,副作用可控。这些结果表明,SEL-212为慢性难治性痛风患者提供了一种新的、有效的治疗选择,有助于改善患者的生活质量并减少痛风相关并发症的发生。
10、Vepdegestrant(ARV-471)
Vepdegestrant由Arvinas公司和辉瑞合作开发,可能成为首个蛋白降解靶向嵌合体(PROTAC)药物,主要用于治疗雌激素受体阳性(ER+)、人表皮生长因子受体2阴性(HER2-)的乳腺癌。
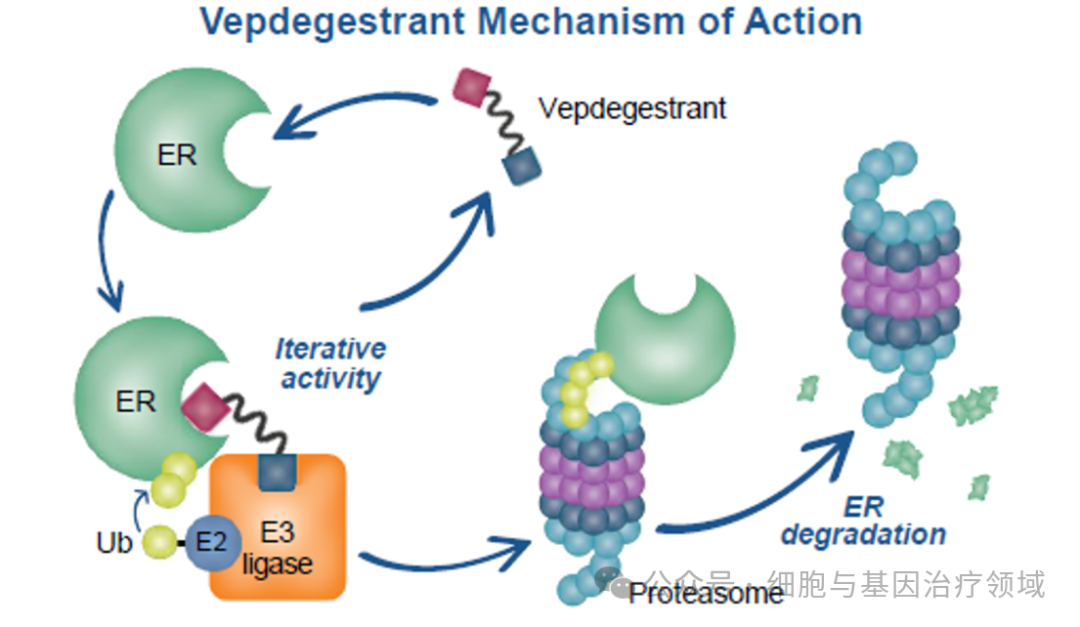
该药物通过利用细胞自身的蛋白质降解机制,特异性地结合并降解雌激素受体,从而阻断癌细胞的生长信号传导路径。临床试验数据显示,在I期和II期临床研究中,Vepdegestrant在经治的ER+/HER2-晚期或转移性乳腺癌患者中表现出显著的抗肿瘤活性和良好的耐受性。例如,在一项II期扩展队列研究中,接受Vepdegestrant单药治疗的患者显示出可观的临床获益率(CBR),部分患者的肿瘤缩小明显,并且药物对多种突变类型的雌激素受体均有效。此外,Vepdegestrant的安全性数据也较为积极,常见的副作用包括恶心、疲劳和食欲下降等,且大多数为轻度至中度。这些结果表明,Vepdegestrant作为一种新型的乳腺癌治疗药物,为那些对现有内分泌疗法产生耐药性的患者提供了新的希望,具有潜在的重要临床应用价值。
11、Zanzalintinib(XL092)
Zanzalintinib由Exelixis开发,是新一代口服酪氨酸激酶抑制剂,可用于治疗结直肠癌、肾细胞癌和头颈鳞状细胞癌。
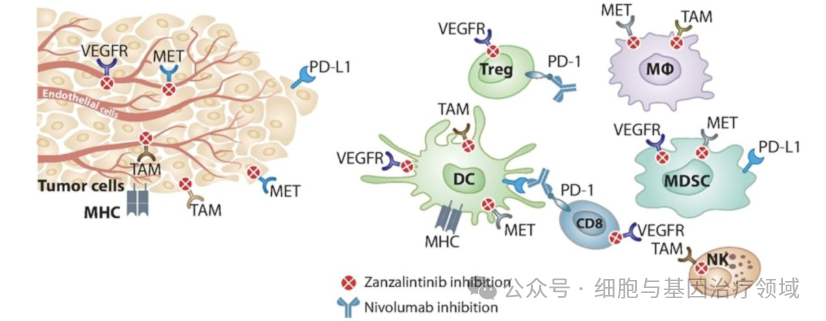
Zanzalintinib是一种多靶点酪氨酸激酶抑制剂,靶向参与肿瘤生长和免疫抑制的VEGF受体、MET和TAM激酶。Zanzalintinib通过抑制这些关键的酪氨酸激酶受体,阻断癌细胞生长和血管生成相关的信号传导路径,从而抑制肿瘤的生长和扩散。当前正在开展针对非透明细胞肾细胞癌(nccRCC)、结直肠癌(CRC)以及头颈部鳞状细胞癌(SCCHN)的III期临床试验。预计zanzalintinib将率先获得美国食品和药物管理局(FDA)的批准,用于治疗nccRCC。与CABOMETYX®(cabozantinib)相比,zanzalintinib可能展现出一定的优势,例如更有可能获得针对nccRCC的监管批准,并适用于更广泛的患者群体。