2021年5月CDE药品审评情况分析报告
来源:药智网 | 发布时间:2021-06-07
摘要:2021年5月份CDE共承办新的药品注册申请以受理号计有820个,其中化药受理614个,中药受理75个,生物制品受理131个。
看点:
- 5月药审中心受理总量为820个(不计复审)。
- 5月46个化药1类新药品种获CDE受理。
- 5月新增74个按仿制药质量和疗效一致性评价品种申报的受理号
根据药智数据最新统计,2021年5月份CDE共承办新的药品注册申请以受理号计有820个(复审除外,下同)其中化药受理614个,中药受理75个,生物制品受理131个;2021年1-5月各类药品注册申请受理情况详见图一。
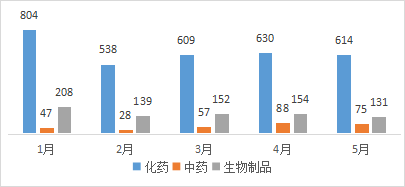
图一 2021年1-5月CDE药品受理情况
数据来源:药智数据,药智咨询整理
以下且看化药、中药、生物制品的注册受理及审评情况详细分析。
一、化药审评情况
5月份CDE共承办新的化药注册申请以受理号计有614个,主要申请类型还是以补充申请为主,数量与上月持平,受理号329个,其次为仿制申请,受理号107个,其中新药申请数量降低,共有受理号77个;2021年1-5月CDE化药各申请类型受理情况详见图二。
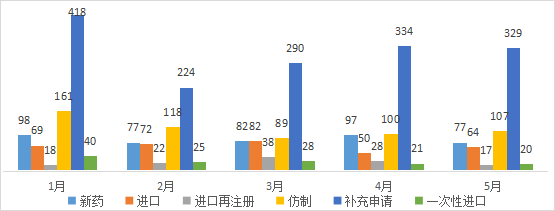
图二 2021年1-5月CDE化药各申请类型受理情况
数据来源:药智数据,药智咨询整理
1.化药1类国产申报情况
5月CDE受理化药国产1类新药共计59个(按受理号计),其中是IND申请56个,NDA申请3个,涉及33个品种31家企业;下表为5月新承办的1类国产新药。
表一 2021年5月新承办的化药1类国产新药
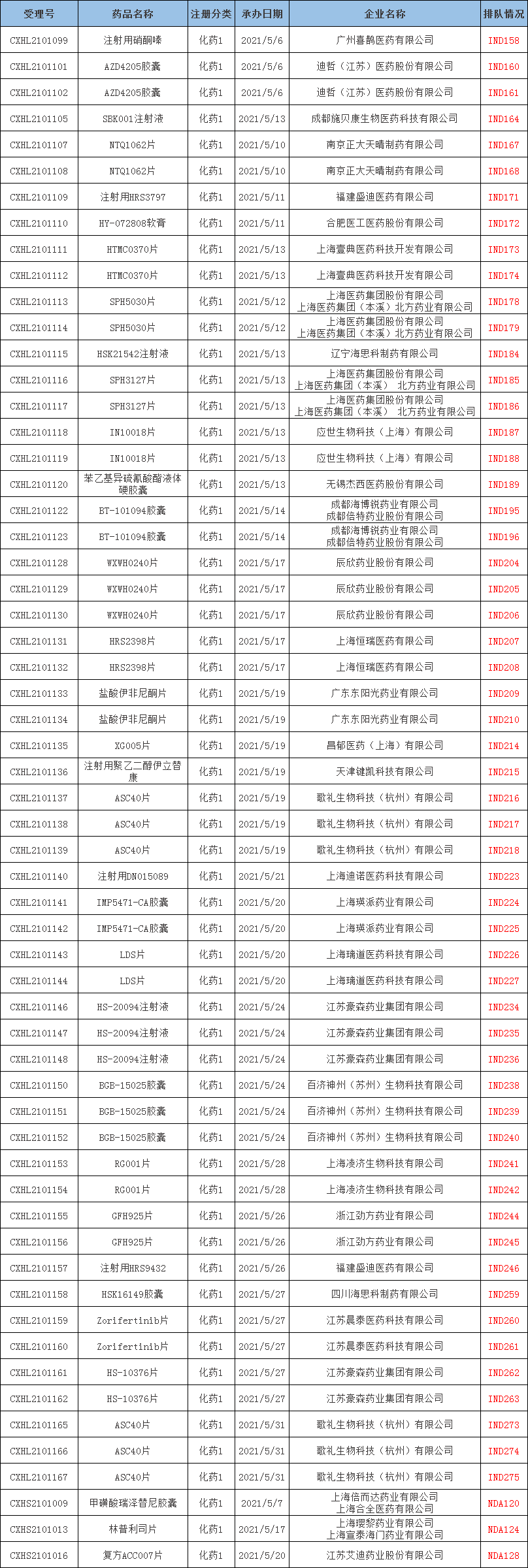
注:排队序号截止至2021年06月03日。
数据来源:药智数据,药智咨询整理
2.化药1类进口药品申报情况
5月共29个进口化药1类受理号获得承办,其全是IND申请,涉及13个品种13家企业;下表为5月新承办的1类进口新药。
表二 2021年5月新承办的化药1类进口新药

注:排队序号截止至2021年06月03日
数据来源:药智数据,药智咨询整理
SPH5030 片
SPH5030 由上海医药自主研发,并拥有完全知识产权的1类创新药,于2019 年 7 月启动立项,2020 年 12 月完成临床前研究,累计投入研发费用约 2500.94 万元人民币;SPH5030是一种新型小分子抑制剂,拟用于晚期实体瘤的治疗;目前已有与SPH5030项目同类的药品在全球上市。
HSK21542注射液
HSK21542注射液是全新的具有自主知识产权的1类创新药物,拟用于急慢性疼痛、瘙痒等适应症的治疗。“急慢性疼痛”适应症于2019年12月获许进入临床,III期临床试验方案于2021年3月获得CDE同意;“瘙痒症”适应症于2020年5月获许进入临床,此次获得受理的适应症为“肝病瘙痒”。HSK21542注射液于2019年10月-2020年10月在澳洲开展了I期临床试验;2020年1月-2020年9月在中国开展了I期临床试验;2020年6月-2021年2月在中国开展了用于腹部腔镜手术术后镇痛的II期临床试验,目前正在进行该适应症的III期临床试验;除此外,HSK21542目前还在开展在血液透析受试者中的II期临床试验。
SPH3127 片
SPH3127由上海医药和日本田边三菱制药株式会社合作研发,双方共同拥有知 识产权的1类创新药。项目于 2019 年 5 月启动立项,2020 年 10 月完成临床前研究,目前高血压适应症正在中国开展Ⅲ期临床试验,轻度至中度溃疡性结肠炎适应症正在美国开展 II 期临床试验,本次药品申报拟开展适应症为慢性肾病的临床试验;目前全球尚无同靶点同适应症的药品上市。
ASC40片
申请的ASC40联合贝伐珠单抗治疗複发性胶质母细胞瘤(rGBM)患者的临床试验申请NMPA已受理;在美国(国外代号为TVB-2640)完成的ASC40联合贝伐珠单抗治疗高级別星形细胞瘤首次複发患者即複发性胶质母细胞瘤患者的II期临床试验取得积极结果(临床试验註册编号:NCT03032484),II期临床试验数据显示ASC40加贝伐珠单抗的总应答率(ORR)为65%,包括20%的完全应答(CR)和45%的部份应答(PR);ASC40联合贝伐珠单抗观察到的6个月无进展生存期(PFS6)为47%,相比较过往贝伐珠单抗单药治疗的历史数据(BELOB16%),6个月无进展生存期(PFS6)在统计学上有显着改善(P =0.01)。
BGB-15025胶囊
BGB-15025胶囊是百济神州的first-in-class HPK1抑制剂,属于1类创新药,本次临床申请适应症为治疗实体瘤。
GFH925片
GFH925片是劲方药业申请临床试验的1类创新药,作用靶点是KRAS G12C,拟被开发用于治疗NSCLC等实体瘤。目前国内外还没有该靶点靶向药物获批上市,但已有多款药物处于临床试验阶段,包括安进的sotorasib(AMG 510)、Mirati Therapeutics公司和诺华合作的Adagrasib(MRTX849)、礼来的LY3537982、Araxes 公司(wellspring公司的子公司)的ARS-3248、贝达药业的BPI-421286等;其中安进的sotorasib(AMG 510)进展最快,已于去年12月先后在美国和欧洲递交上市申请,适应症为先前已接受过至少一种系统疗法、经FDA批准的检测方法证实存在KRAS G12C突变、局部晚期或转移性NSCLC,其中在美国还被FDA授予优先审查资格。
HSK16149胶囊
HSK16149胶囊是四川海思科制药有限公司自主研发,并拥有HSK16149的专利在中国境内的独占实施许可权的1类创新药,目前拟用于治疗糖尿病周围神经痛及带状疱疹后神经痛等适应症。品种于2019年10月获得适应症为“糖尿病周围神经痛和带状疱疹后神经痛”的临床批件,本次受理的适应症为“辅助镇痛”。
林普利司片
林普利司片是上海璎黎药业有限公司自主研发的1类创新药,拟用于治疗复发/难治滤泡性淋巴瘤。在国内,还没有同靶点的上市药物,但已有两款药物获得了CDE优先审评资格,分别为Copanlisib和度恩西布。
复方ACC007片
复方ACC007片是全新结构的非核苷类逆转录酶抑制剂,为公司首个抗艾滋病1类新药,被列入国家十三五“重大新药创制”科技重大专项。目前已经完成III期临床试验,试验结果良好、到达主要临床终点指标。
二、中药审评情况
5月份CDE承办新的中药注册申请受理号共计75个,其中新药3个,补充申请72个;2021年1-5月CDE中药各申请类型受理情况详见图三。
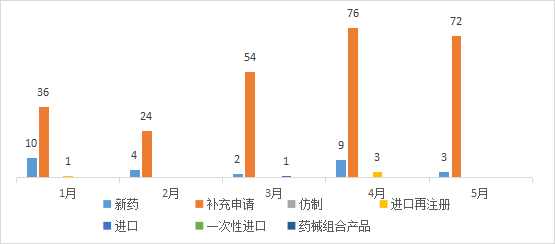
图三 2021年1-5月CDE中药各申请类型受理情况
数据来源:药智数据,药智咨询整理
5月共3个中药1类创新药受理号获得承办,均为IND申请;下表为5月新承办的中药1类创新药。
表三 2021年5月新承办的中药1类创新药
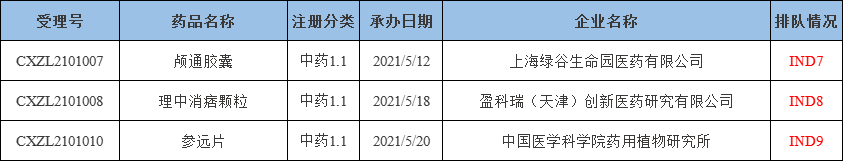
注:排队序号截止至2021年06月01日
数据来源:药智数据,药智咨询整理
三、生物制品审评情况
5月份CDE承办新的生物制品注册申请受理号共计131个,新药53个,补充申请56个,进口18个,进口再注册4个;2021年1-5月CDE生物制品各申请类型受理情况详见图四。
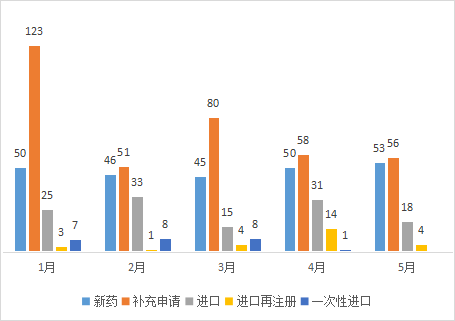
图四 2021年1-5月CDE生物制品各申请类型受理情况
数据来源:药智数据,药智咨询整理
5月有37个1类治疗用生物制品受理号获得承办,全为临床试验申请,目前均已经进入相应序列排队待审;下表为5月新承办的生物制品1类创新药。
表四 2021年5月新承办的治疗用生物制品1类新药
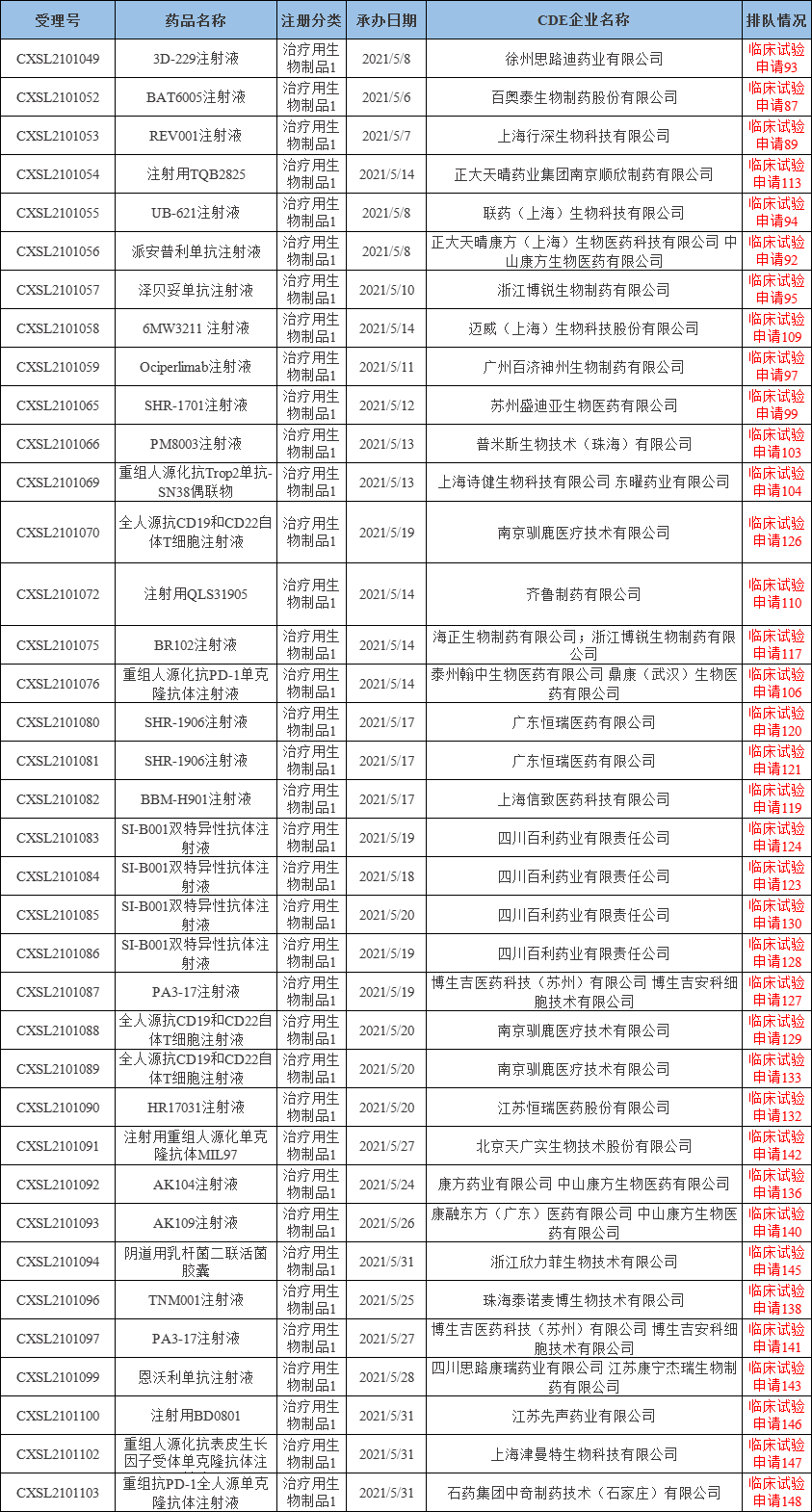
注:排队序号截止至2021年06月03日。
数据来源:药智数据,药智咨询整理
四、按一致性评价申报品种情况
5月新增74个按一致性评价要求进行申报的受理号和114个视同受理号。(篇幅限制仅展示一致性信息,视同及具体信息请关注药智企业版药品注册与受理数据库);2021年1-5月一致性评价受理数量详见图五;表五为5月新增一致性评价受理号信息。
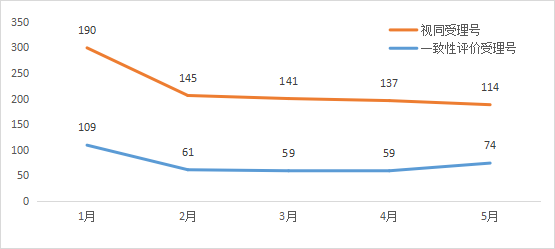
图五 2021年1-5月一致性评价受理数量
数据来源:药智数据,药智咨询整理
表五 2021年5月新增一致性评价受理数据
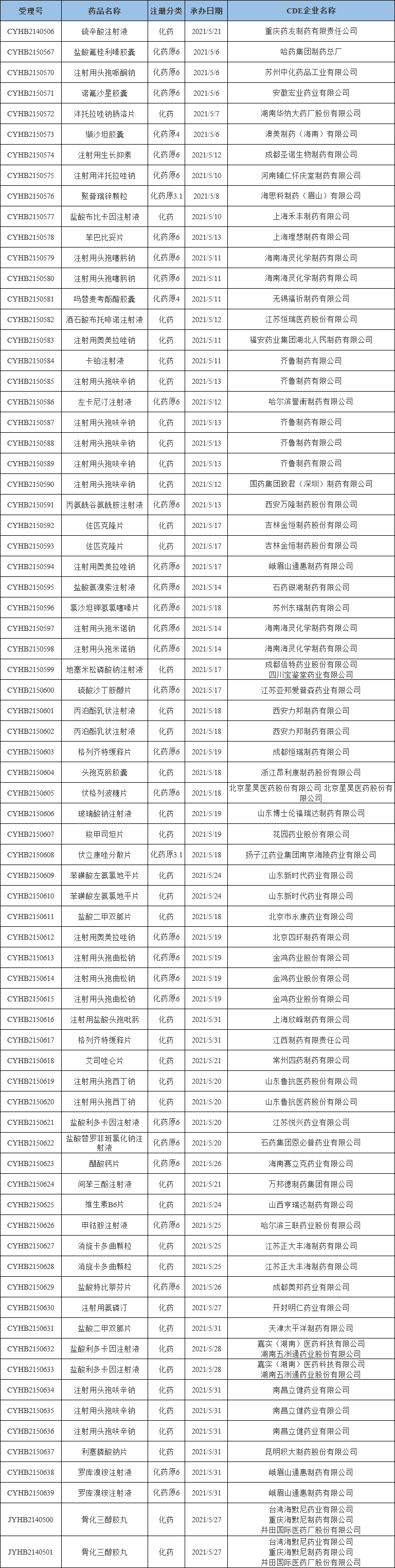
数据来源:药智药品注册与受理数据库,药智咨询整理