GLP-1R药物交易盘点
来源:药智网 | 发布时间:2024-10-08
摘要:GLP-1R药物因司美格鲁肽和替尔泊肽的成功而备受市场追捧,2019至2024年交易额增长595%,达122亿美元。中国药企如恒瑞医药、诚益生物等通过许可交易推动GLP-1R药物出海,同时引进国外管线。当前研发趋势集中在提高疗效、延长给药间隔、拓展适应症及口服给药,以期在减重市场中抢占份额。活跃的交易促进创新,有望加速新一代GLP-1R药物崛起。
近年来,司美格鲁肽和替尔泊肽在肥胖治疗领域的成功,极大地激发了市场对胰高血糖素样肽-1受体(GLP-1R)药物的兴趣,针对GLP-1R药物的交易火热。
GLP-1R药物交易火热
据行业知名媒体GlobalData统计,2019年~2024年间,针对GLP-1R药物的交易金额增长了595%,仅2024年就已达成超过62亿美元的交易额。GlobalData分析师Alison Labya评论道:“制药公司正将赌注押在GLP-1R激动剂上,试图挑战诺和诺德和礼来。”
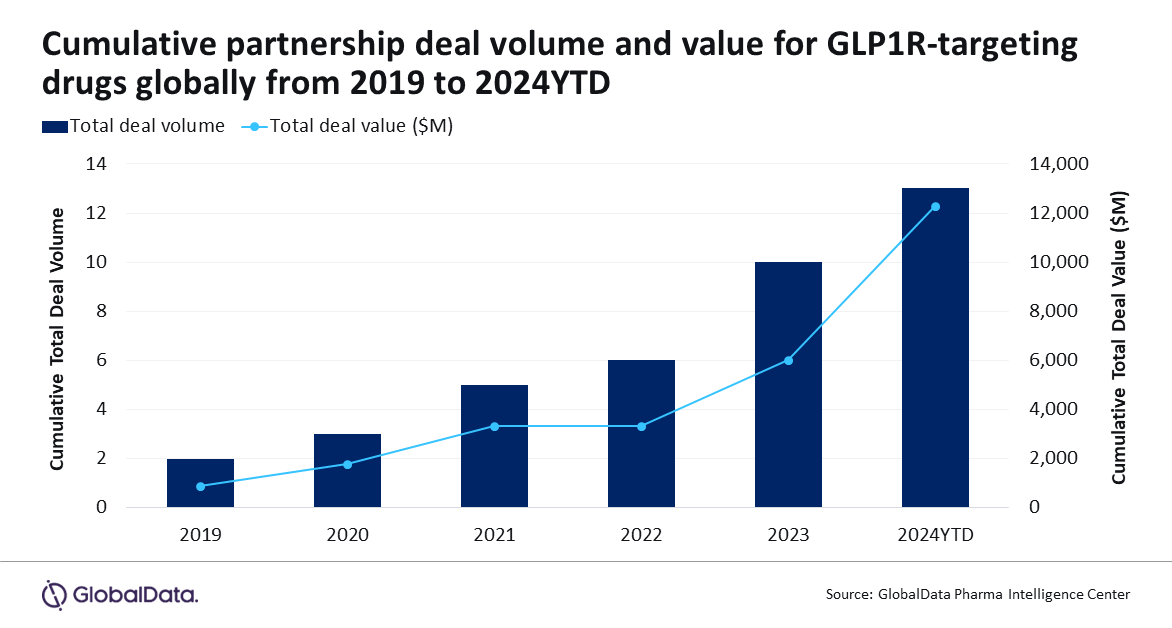
图片来源:参考资料
根据GlobalData数据,2019年至今,针对GLP-1R的药物的许可交易总金额达到122亿美元。
从研发阶段来看,三分之二的项目处于I期至III期临床试验阶段,三分之一处于临床前阶段。
从适应症来看,代谢紊乱是GLP-1R靶向药物许可交易的主要疾病领域,2019年至今的总交易额达到105亿美元。其次为心血管领域,许可交易总额为60亿美元,胃肠疾病为45亿美元,这也意味着,GLP-1R药物的适应症已扩展到2型糖尿病和肥胖之外的疾病。
国产GLP-1药物出海各显神通
据药智数据,目前全球在研GLP-1药物有约270款,其中近一半由中国药企贡献。庞大的在研管线数量吸引全球药企来中国采购GLP-1管线。
2022年至2024年期间,针对GLP-1R药物的许可交易呈现复苏趋势,而中国药企为这一复苏贡献了不少力量,例如恒瑞医药在今年就贡献了60亿美元的交易额。
表1 涉及中国药企的GLP-1药物许可交易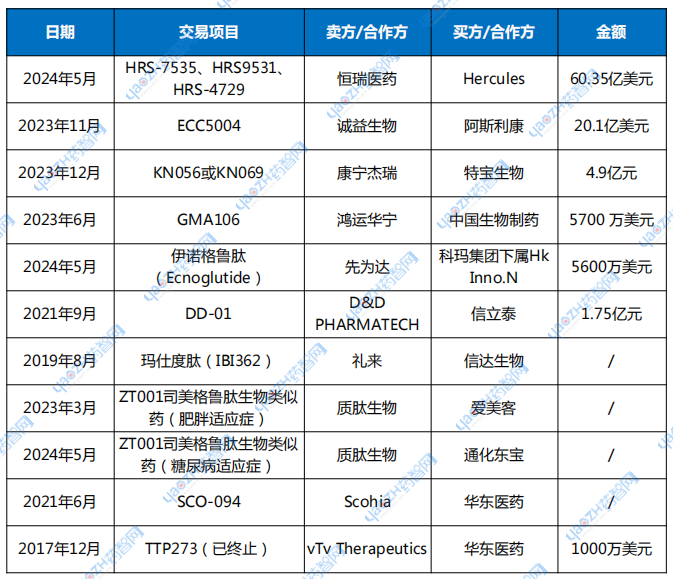
数据来源:根据公开资料整理
2024年5月,中国制药巨头江苏恒瑞医药将其GLP-1R药物组合的中国以外权利授权给新成立的美国生物技术公司Hercules。
根据协议,Hercules公司将向恒瑞医药支付首付款和近期里程碑款总计1.1亿美元,临床开发及监管里程碑款累计不超过2亿美元,销售里程碑款累计不超过57.25亿美元,及销售提成。作为对外许可交易对价一部分,恒瑞医药还将取得美国Hercules公司19.9%的股权。
该项许可交易涉及3款GLP-1R创新药——HRS-7535、HRS9531和HRS-4729。
HRS-7535是一款口服小分子GLP-1R激动剂。目前,该药用于2型糖尿病已进入临床Ⅲ期,减重适应症也已进入Ⅱ期临床。
HRS-9531是一款GLP-1R/GIPR双靶点激动剂,用于超重或肥胖适应症已进入Ⅲ期临床。
HRS-4729是一款下一代肠促胰岛素产品,目前处于临床前开发阶段。
在此之前,2023年11月,中国biotech公司诚益生物与阿斯利康就小分子GLP-1R激动剂ECC-5004达成一项超20亿美元的独家许可协议。
根据协议,诚益生物将获得1.85亿美元的首付款,还将有资格获得高达18.25亿美元的未来临床、注册和商业化里程碑付款以及特许权使用费。阿斯利康将获得ECC5004在中国以外的所有地区的独家开发和商业化权利,适应症包括用于包括肥胖症、2型糖尿病和其他合并症的潜在治疗。
ECC5004是诚益生物开发的一种每日一次口服的GLP-1受体激动剂(GLP-1RA),目前其2型糖尿病和肥胖适应症均已进入临床Ⅱ期阶段。
此外,先为达生物的长效GLP-1R激动剂伊诺格鲁肽注射液(Ecnoglutide,XW003)也在2024年成功出海韩国。目前,伊诺格鲁肽用于糖尿病、肥胖、MASH三个适应症均已进入临床Ⅲ期研究。
“引进”同样重要
从表1可以看出,国产GLP-1药物除了参与跨境license out交易,国内企业间的交易也很火热,另外国内企业也在积极将国外潜力管线引进中国。
玛仕度肽(IBI362)
2019年8月,信达生物从礼来引进玛仕度肽(IBI362,OXM3)的中国权益,目前该药被信达视为下一个核心产品。
玛仕度肽是一款GLP-1R/GCGR双靶激动剂,它利用脂肪酰基侧链延长作用时间,允许每周给药一次。
根据玛仕度肽高剂量9 mg在中国肥胖受试者中的Ⅱ期临床48周数据,玛仕度肽减重效果、安全性都优于司美格鲁肽和替尔泊肽。
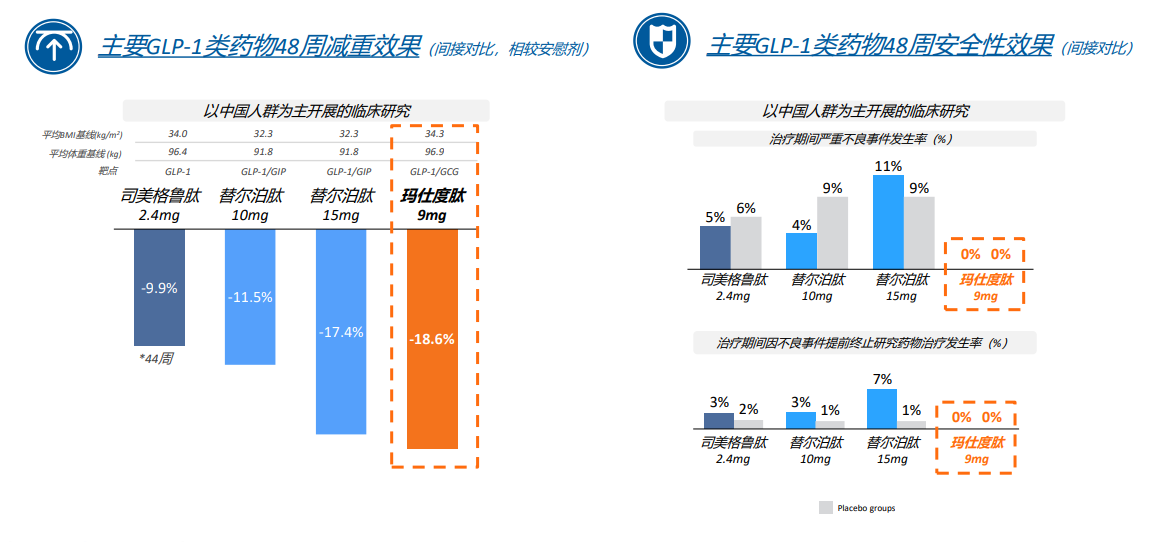
图片来源:信达生物
治疗48周后,玛仕度肽9 mg组体重较基线的平均百分比变化与安慰剂组的治疗差值达−18.6%,平均变化值与安慰剂组的差值达−17.8 kg。在安全性上,玛仕度肽高剂量9mg治疗48周,无受试者因不良事件提前终止研究药物治疗,未发生严重不良事件。
2024年2月,玛仕度肽首个NDA获得CDE受理,用于肥胖或超重患者长期体重管理。其余在研适应症包括糖尿病、代谢性脂肪肝病(MASH)、青少年肥胖等。
DD01
2021年9月,信立泰从韩国D&D Pharmatech公司引进DD01在中国大陆地区的独家许可权,该合作涉及金额超1.75亿元。
DD01也是一款GLP-1R/GCGR双靶激动剂,目前该药正在美国开展治疗肥胖和超重患者的Ⅱ期临床试验。
SCO-094
2021年2月,华东医药从日本SCOHIA公司引进SCO-094在亚太国家和地区(不含日本)的独家开发、生产及商业化权益。2023年,华东医药又将合作范围进一步扩大,获得SCO-094及其衍生产品在全球(包括日本)的独家开发、生产及商业化权益。
SCO-094是一种GLP-1R/GIPR双靶点药物,正在开展针对肥胖、糖尿病、代谢性脂肪性肝炎的Ⅰ期临床试验。
GMA106
2023年6月,中国生物制药与鸿运华宁达成合作协议,将共同开发双靶点减重创新药GMA106。鸿运华宁将从交易中获得最高5700万美元的首付款与里程碑付款。
GMA106是一种GLP-1R/GIPR双靶点药物,与安进公司的在研产品AMG133机制相似,均是抑制GIPR而激活GLP-1R。
GMA106在澳洲进行的I期临床试验显示出良好的耐受性与安全性,而且显示出体内半衰期长,停药后可防止反弹等优点,有望成为新一代减重、减脂、停药防反弹的候选减肥药物。
KN056/KN069
2023年12月,康宁杰瑞与特宝生物就KN056或KN069达成许可协议,特宝生物向苏州康宁杰瑞支付累计最高人民币4.9亿元的权益付款,获得KN056或KN069的中国大陆地区许可权利。
KN069是一种重组人GLP-1变体/GIPR人源化单域抗体Fc融合双功能蛋白。该药物同时表现出GLP-1受体激动剂活性和GIPR拮抗剂活性,通过协同作用实现体重和血糖的双重调控。目前,KN069正在中国开展超重/肥胖适应症的Ⅰ期临床试验。
KN056是一种GLP-1受体激动剂融合蛋白。基于独特的蛋白质工程技术,相较于现有的周剂型GLP-1激动剂,KN056具有显著延长的体内半衰期。KN056已分别在中国及新西兰的健康受试者中开展2型糖尿病的Ⅰ期临床试验。
GLP-1药物迭代进行时
诺和诺德的GLP-1R激动剂Wegovy/Ozempic(司美格鲁肽)在2023年销售额已达212亿美元,2024年上半年司美格鲁肽销售额再次实现同比大增,达到130亿美元,是今年全球“药王”的有力竞争者。
礼来的双重GLP-1R/GIPR激动剂Mounjaro/Zepbound(替尔泊肽)今年上半年销售额也已达66.58亿美元,增长速度令市场震惊。
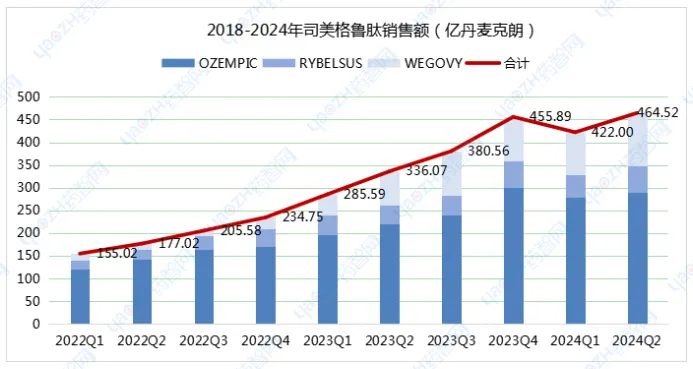
数据来源:诺和诺德财报
在两款明星药物的加持下,全球GLP-1R药物研发火热。根据药智数据,目前全球在研GLP-1R药物约有270款,各大药企纷纷押注新型GLP-1R药物,希望赶超司美格鲁肽、替尔泊肽,在广阔的减重市场分得一杯羹。
目前针对GLP-1R药物的改进方向主要包括提高疗效,延长给药间隔,拓展糖尿病和肥胖症之外的适应症,以及口服给药。
活跃的交易有利于促进创新,加速药物迭代,期待新一代GLP-1R药物崛起。