分子胶产业动态报告出炉
来源:药明康德 | 发布时间:2024-03-26
摘要:分子胶的小分子量及其调控蛋白质间相互作用(PPI)的能力,以及更易于成药的特性使其成为近年来产业界密切关注的新型治疗模式。近日,《自然》子刊Nature Biotechnology针对分子胶降解剂在产业界的开发现状发布了报道,本文向读者展示分子胶领域的最新产业动态。
分子胶的小分子量及其调控蛋白质间相互作用(PPI)的能力,以及更易于成药的特性使其成为近年来产业界密切关注的新型治疗模式。近日,《自然》子刊Nature Biotechnology针对分子胶降解剂在产业界的开发现状发布了报道,本文向读者展示分子胶领域的最新产业动态。
分子胶概述及其研发挑战
分子胶是一类单价小分子(<500 Da),能够改变E3连接酶的表面结构,从而促进新的蛋白质-蛋白质相互作用。与蛋白降解嵌合体(PROTAC)相比,分子胶因其较小的分子量而更易于细胞吸收,并且可以在较低剂量下发挥作用。不同于靶向PROTAC采用灵活连接子(linker)连接两个配体、并允许它们扭曲和转动以形成接触点的方式,分子胶降解剂通过更直接地介入蛋白质界面,加强E3连接酶与靶蛋白之间的复合物形成,从而诱导它们之间的亲和力增加,最终导致靶蛋白的泛素化与降解。
目前最广为人知的分子胶降解剂是沙利度胺(thalidomide)及其类似物泊马度胺(pomalidomide)等获批的免疫调节药物(IMiD),它们能与CRL4CRBN E3泛素连接酶中的底物受体蛋白cereblon(CRBN)相结合,通过改变CRBN所靶向底物蛋白的特性,使得CRL4CRBN E3泛素连接酶得以与新的底物蛋白相连并诱导该蛋白后续的降解。
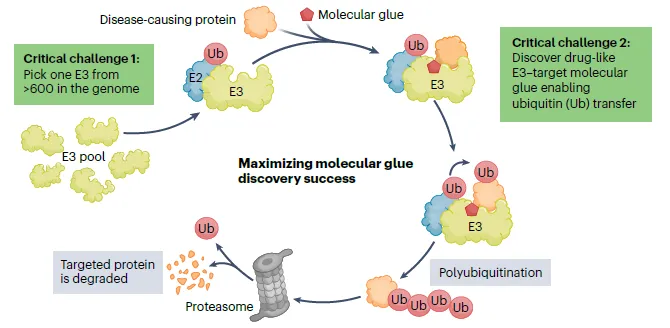
▲分子胶作用原理图示(图片你来源:参考资料[1])
然而,开发创新的分子胶降解剂面临着不少挑战。首先,分子胶降解剂的初步筛选必须在细胞环境中完成,这不仅提高了成本、增加了时间消耗,还需要大量的后期验证工作。人体内存在600多种E3连接酶,从中挑选出适合降解特定目标蛋白的连接酶颇具挑战性,尤其是考虑到科学家对这些连接酶中的仅20-30种有较深入的生物学理解,这为发现新的分子胶增加了难度。此外,找到能够促使E3连接酶与目标蛋白互动的小分子的几率较低,并且目前对分子胶的一般化学特性的了解尚浅,这些因素均提高了化合物库筛选的复杂性,通常需要依赖大型的化合物库才有可能找到合适分子。
分子胶疗法领域的弄潮儿
尽管分子胶类药物的开发过程不易,仍有不少公司勇敢地接受了这一挑战,通过不同研发策略来开发潜在的分子胶药物,尤其是针对难以成药的蛋白,像是转录因子这样缺乏可供小分子药物结合口袋结构的蛋白。这些专注于分子胶疗法开发的公司及其策略主要包含:
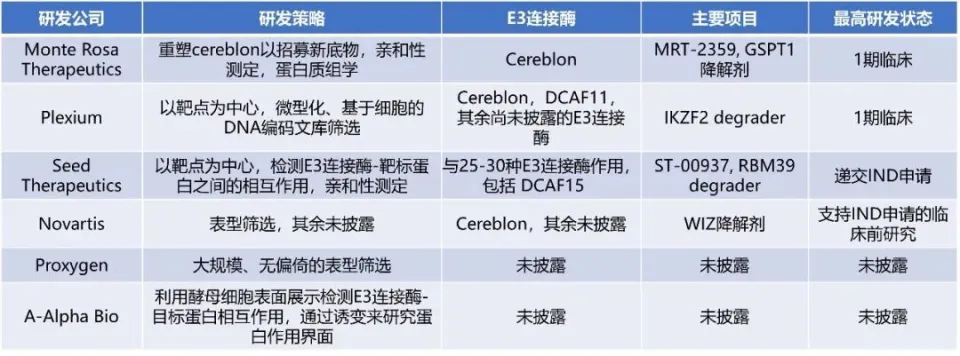
▲专注于分子胶疗法研发的部分公司名单(图片来源:药明康德内容团队根据参考资料[1]制表)
Monte Rosa Therapeutics
Monte Rosa Therapeutics专注开发利用cereblon E3连接酶降解特定靶标蛋白的分子胶疗法。该公司的联合创始人Raj Chopra先生在Celgene公司工作期间,曾带领团队成功鉴定了首批cereblon降解底物,并展现了通过合理方法发现其新底物的巨大潜力。
Monte Rosa公司的核心理念是通过使用不同的分子胶来改变cereblon的表面结构,从而招募并降解多种蛋白质。这些cereblon底物蛋白中,大部分是带有被称作“G环”的降解结构的锌指转录因子。Monte Rosa利用人工智能工具来预测不同小分子如何重新塑造cereblon的表面,使其能够招募并降解含G环的转录因子及其他蛋白质。基于已知的cereblon-分子胶复合体晶体结构,公司合成了这类分子,并在蛋白质和细胞层面进行筛选,通过生化和细胞亲和性测定来鉴定被降解的蛋白质,以验证蛋白间的相互作用,并利用蛋白质组学技术来验证降解事件并确保其特异性。
Monte Rosa的首席战略官Owen Wallace博士透露,通过筛选,Monte Rosa已经鉴定出与cereblon结合的新靶点,这些靶点的结合方式与预期不同。公司目前正在研究的两个项目分别针对cdk2和Vav1,这两个靶点都不包含传统的G环结构。这一发现表明,通过引导cereblon识别非传统靶点的方法是可行的,并且其潜在的靶标空间仍在不断扩展。
Proxygen
Proxygen公司开发了一种功能强大的专有技术平台,专注于大规模识别针对难治性或传统手段难以作用的靶点的分子胶降解剂。Proxygen高度通用、专有的发现引擎,支持针对难以成药或不可成药靶点的分子胶降解剂的大规模特异性和无偏倚的筛选。公司的首席执行官Bernd Boidol博士表示,仅依赖结构方法无法揭示所有的作用机制,因此公司旨在深入了解分子胶降解剂和E3连接酶之间的生物学机理,以推动该领域的发展。同时,Proxygen通过结合精准的靶点选择和临床验证来平衡技术与生物学风险。
Seed Therapeutics
Seed Therapeutic强调在分子胶药物开发中选择恰当的E3连接酶的重要性。公司的研发流程从评估靶蛋白与E3连接酶之间的互补性开始,利用AlphaFold等计算技术,并考虑E3连接酶在细胞内的位置;然后在细胞模型中研究E3连接酶与靶蛋白的相互作用;验证E3连接酶对靶蛋白的泛素化能力;随后通过高通量筛选来发现合适的降解剂,并进行验证;最终通过药物化学研究来提高药物的效能、特异性和稳定性。Seed Therapeutics的总裁及首席科学官James Tonra博士指出,选择一个能够经受包括高通量筛选和基于细胞的活性测试等所有检验的E3连接酶,是避免在长期研发结束后因需更换E3连接酶而重复研究的关键。
A-Alpha Bio
A-Alpha Bio是一家运用合成生物学和机器学习技术来测量、预测和设计蛋白质之间相互作用的生物技术公司。该公司拥有两个核心技术平台:AlphaSeq能够快速且定量地测量数百万种蛋白质间的结合亲和力;而AlphaBind则是一个计算平台,它使用全球最大型之一的蛋白质相互作用数据库进行训练,能够基于序列预测蛋白质结合强度。
A-Alpha Bio公司采用了一种高通量酵母细胞表面展示系统来测试蛋白之间的相互作用。通过将目标蛋白与酵母的锚定蛋白以及参与蛋白质分泌的信号肽序列融合,工程化改造后的酵母细胞能够在其表面表达各种细胞内部蛋白。这些酵母细胞在液体培养中混合并振荡,通过蛋白-蛋白相互作用引导的细胞融合来筛选相互作用的蛋白对。随后对产生的二倍体细胞进行测序,以确定参与相互作用的蛋白质,并通过生物物理验证实验进一步确认。接着,公司会对蛋白-蛋白界面进行突变实验,以探究增强这些相互作用的可能性。A-Alpha Bio的最终目标是通过优先识别和改进现有的蛋白质相互作用,来增加发现有效分子胶的成功率。
Plexium
Plexium是一家新一代靶向蛋白降解(TPD)疗法研发公司,致力于开发单价直接降解剂和分子胶,针对治疗癌症中难以攻克的靶点。公司专有的药物发现平台旨在发现新型小分子药物,通过E3连接酶介导的蛋白酶体降解途径,诱导致病蛋白的选择性降解。
Plexium的平台将“on-bead”DNA编码文库(DEL)筛选技术与超高通量微型化细胞检测相结合,能够在与疾病相关的细胞环境中直接测量一个或多个目标蛋白的降解情况。Plexium正在利用其平台来鉴定针对致病蛋白的单价降解剂或分子胶降解剂。Plexium旗下多款分子胶研发项目正在积极推进,其中PLX-4545已进入临床开发阶段。
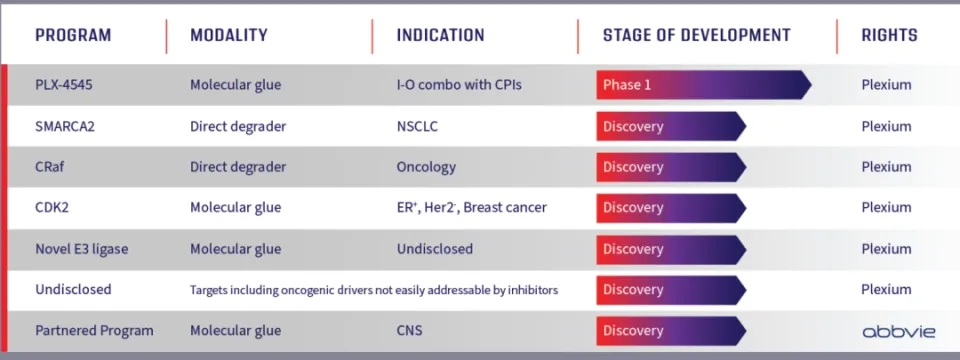
▲Plexium公司研发管线(图片来源:Plexium公司官网)
诺华(Novartis)
诺华公司也在分子胶领域有所布局,专注于开发针对转录因子WIZ的分子胶降解剂。在美国血液学会年会上,该公司报告了两种新型降解剂dWIZ-1和dWIZ-2的研发成果。dWIZ-1是通过针对CRBN的化学库进行表型筛选获得的,筛选标准是寻找能促进胎儿血红蛋白(HbF)表达而不影响红系细胞增殖和分化的化合物。后续的蛋白质组学分析确认了WIZ为其靶点。
诺华的dWIZ-2是基于dWIZ-1优化后的分子,因其优良的药物动力学属性而适用于体内WIZ降解和HbF诱导的评估。在体外实验中,dWIZ-2显著增加了镰状细胞病患者来源的红系细胞的HbF表达。利用人源化小鼠模型对dWIZ-2的体内效应进行评估时,显示其能剂量依赖性地降解WIZ并提高HbF水平。
在动物模型中,连续28天每日口服dWIZ-2治疗后,观察到外周血中γ-珠蛋白mRNA水平和HbF阳性网织红细胞比例显著增加。此外,dWIZ-2具有良好的耐受性,未观察到任何与治疗相关的血液学、凝血或临床化学指标的变化。这些研究成果支持将口服WIZ降解剂作为治疗镰状细胞病的新策略。
近年大型药企在分子胶领域的布局
分子胶疗法的发展被广泛看好,许多大型药企也在这个领域进行布局,并与许多生物科技公司达成合作协议。例如,Proxygen分别在2020年、2022年、2023年与勃林格殷格翰(Boehringer Ingelheim)、德国默克(Merck KGaA)和默沙东(MSD)达成共同开发分子胶降解剂的协议。而Monte Rosa Therapeutics公司则在去年10月与罗氏(Roche)达成合作,将共同针对此前被认为不可成药的癌症和神经疾病靶点共同开发分子胶药物。
此外,Orionis Biosciences也在去年9月宣布与罗氏(Roche)旗下基因泰克(Genentech)达成金额高达20亿美元的多年合作,将共同针对重大疾病领域中的挑战性靶点发现新型分子胶药物,包括肿瘤学和神经退行性疾病。今年2月,百时美施贵宝(Bristol Myers Squibb)与VantAI达成战略合作,将共同针对某些治疗靶点发现新的分子胶。此次合作利用VantAI的几何深度学习能力和百时美施贵宝在靶向蛋白质降解方面的专业知识来发现和开发新的小分子疗法。同月,诺和诺德(Novo Nordisk)也与Neomorph达成14.6亿美元的合作,将共同发现、开发和商业化分子胶蛋白降解剂的合作。
尽管在这一创新领域还存在许多挑战,包括需要解析复杂的生物学相互作用和实现精确靶向等,但大型药企的大力投资和生物技术公司的持续关注表明,分子胶疗法具有广阔的发展前景。随着研究人员不断在科学研究上取得新的突破,让我们期待在不久的未来会有更多分子胶降解剂进入临床、造福患者。