罗氏布局类器官技术:新药研发的下一个风口
来源:药智网 | 发布时间:2023-05-11
摘要:全球制药巨头罗氏(Roche)公司宣布成立人类生物学研究所(Institute of Human Biology,IHB),致力于研究类器官(organoid)等人类模型系统。该研究所旨在利用这些模型系统提高对器官功能和疾病的理解,加速药物的研发和发现,最终实现缩短药物上市的时间,让患者从中受益。
近日,全球制药巨头罗氏(Roche)公司宣布成立人类生物学研究所(Institute of Human Biology,IHB),致力于研究类器官(organoid)等人类模型系统。该研究所旨在利用这些模型系统提高对器官功能和疾病的理解,加速药物的研发和发现,最终实现缩短药物上市的时间,让患者从中受益。
那么,什么是类器官技术?会是新药研发的下一个风口吗?
加速新药研发利器:类器官技术
类器官是一种近年来备受瞩目的生物技术,它可以从干细胞中自组装形成具有特定功能和形态的“小器官”,可以作为人体组织的模型用于研究各种疾病和药物反应。
要构建一个类器官,首先需要从干细胞中分化出特定器官的细胞,再通过三维培养技术,使其自组织形成的三维结构。
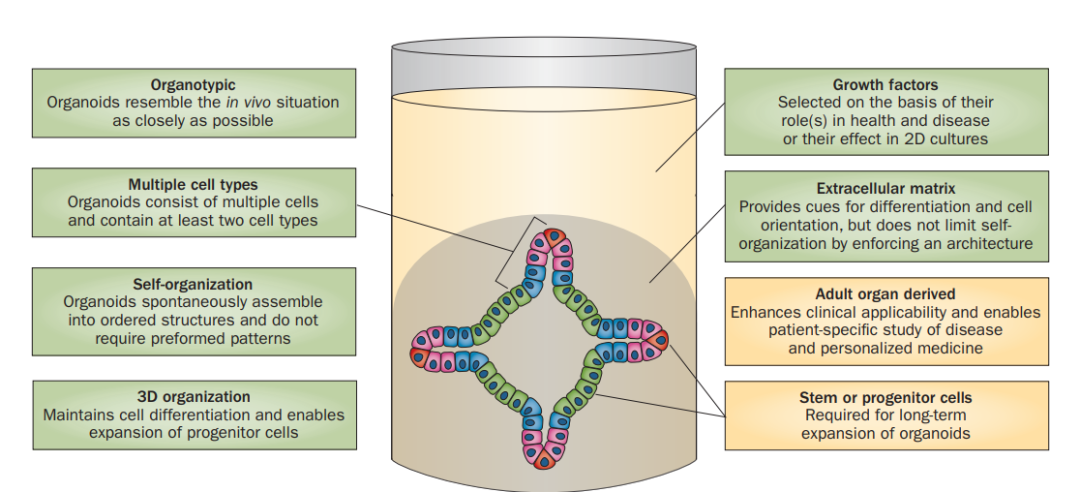
图1 类器官的构建要素及细胞来源
图片来源:Maarten B. Rookmaaker et al., Nature Reviews Nephrology
构建一个类器官一般采用两种类型的干细胞作为“原材料”:(1)多能干细胞PSCs(即胚胎干细胞诱导多能性干细胞),以及(2)器官特异性成体干细胞(ASCs)。这两种方法都利用了干细胞在培养过程中不断扩增并且具备分化的潜力。
近10年来,多种3D培养技术不断更新,通过对细胞外基质和细胞生长因子的优化,利用PSCs和ASCs在培养中分化时可以自组装成具有组织特异性结构的能力,构建出一定大小的类器官,以实现对体内器官的模拟。
目前,体外培养的类器官具有多种类型,包括脑、肾脏、肺、肠道和视网膜等,这些类器官不仅在结构上类似体内组织,而且具有相应的生理功能,这使得类器官技术成了在实验室中模拟人类器官发育和多种病理情况的有效手段。
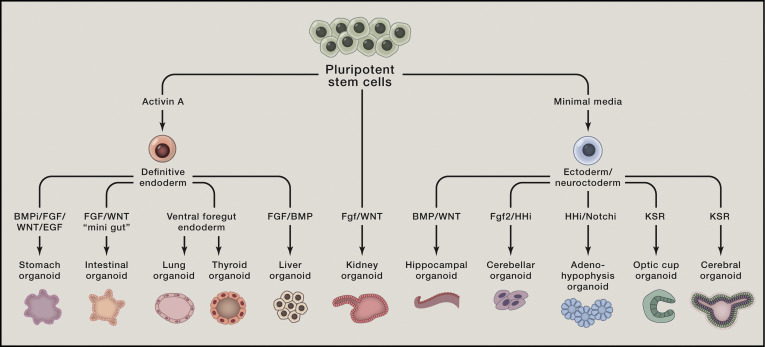
图2 可以从多能性干细胞出发,培养出多种不同的类器官,这些类器官的形成需要特定的生长信号因子,以模拟胚胎器官的发育过程。
图片来源:Hans Clevers et al., Cell
长期以来,药物研发过程低效、缓慢且昂贵。
据统计,在肿瘤治疗药物研发方面,经过临床前研究开发的药物中,只有5%能够在临床试验中展现出效果。这种高淘汰率主要是由于早期试验阶段缺乏优秀的实验模型,目前采用的细胞系和动物模型往往不能准确反映出药物的实际临床效果。因此,优化药物早期试验中使用的实验模型成了推动药物研发机构开发下一代临床前模型的一个重要目标。
在这样的背景下,类器官技术逐渐成为新药研发领域的重要工具之一,其可以在很大程度上减少动物试验的需求,更好地模拟人体的器官特征,加快新药的研发和上市速度。
Hans Clevers加盟罗氏
加速类器官技术布局
在类器官技术用于新药研发浪潮的背景下,罗氏公司早先已经开始类器官研究的布局。2022年2月,罗氏公司聘请了类器官领域的先驱Hans Clevers博士担任罗氏药物研究和早期开发负责人。
在学术界,Hans Clevers是细胞和分子生物学领域的著名科学家,曾经在荷兰的乌德勒支大学和皇家荷兰科学院任职。他的一项开创性研究成果是发现了肠道干细胞,并建立了相应的干细胞培养系统,这项技术被广泛应用于肠道疾病的研究和治疗。
随着类器官技术的发展,Hans Clevers也逐渐将研究重点转向了这个领域。他在类器官技术方面取得了许多重要成果,例如建立了人类肝脏和肾脏等多种类器官模型,这些模型不仅可以用于疾病的研究,还可以作为药物筛选的重要工具。
Hans Clevers加入罗氏后,将负责罗氏药物研究和早期开发的工作。他将领导罗氏在类器官技术方面的研究和开发,并探索如何将这些技术应用于药物研发的各个环节。
图片来源:罗氏官网关于Hans Clevers的介绍
作为全球类器官技术领域的开拓者,Hans Clevers及其团队在该领域的研究成果备受关注。
2013年,Hans Clevers参与创办了类器官技术孵化公司Hubrecht Organoid Technology(HUB),这也是全球类器官最早的研发中心。HUB类器官技术基于Hans Clever实验室发现的Lgr5干细胞实验成果,随后发展出第一款“培养皿中的小肠”技术。HUB类器官技术不需要干细胞的重编程或转化,而是采用了成体干细胞(ASCs)作为构建细胞类型,进而开发出患病和健康的类器官,保留原始组织的基因组和表观遗传学特征。目前,HUB已经开发了一系列标准化的类器官疾病类型,构建了患者来源的类器官活体库,这些类器官在长期培养中是稳定的,可以扩增和冷冻保存用于多种应用。
此外,HUB还开发了一种类器官药物筛选工具,用于开发和验证药物,支持小分子和大分子的疗效筛选,并减少研发化合物所需的时间和成本。
近期发表在《自然癌症》杂志上的一篇论文展示了用结肠直肠癌类器官鉴定了一种引导双特异性抗体,其在开发初期的5年内即达到了临床试验阶段,从而证明了在药物开发中减少和替代动物模型的可行性。

类器官应用类型
图片来源:Hubrecht Organoid Technology官方网站
多家生物公司纷纷布局
类器官技术方兴未艾
与类器官相关的新技术正在以指数级别增长,使其成为了在免疫肿瘤学、炎症性疾病、感染性疾病和毒理学中具有临床相关性的新型临床前模型。
此前,类器官研发企业大多通过出售产品间接为药企提供服务。2015年以后,越来越多的药企通过购买产品、合作授权以及投资等形式直接入场,进一步推动了该领域的发展。
2015年,强生购买Emulate公司的血栓芯片,用于检测其在已上市药物或在研药物中的促血凝特性。
2018年5月,辉瑞与HUB合作开发人类肠道类器官平台,用来研究克罗恩病、溃疡性结肠炎等疾病。
2021年,赛诺菲与Hesperos合作,共同进行NCT04658472临床前研究,并且该项目还是FDA批准的全球首个完全基于“类器官芯片”研究获得临床前数据的新药。
在我国,近年来类器官的研究进展迅速,并且随着资本市场的关注,相关企业得到了多轮融资。
如2022年,创芯国际完成1亿元Pre B轮融资;丹望医疗完成数千万元天使轮融资和1.2亿人民币A轮融资。
药企方面,百济神州与创芯国际签署战略合作协议,共同建立类器官新药研发技术平台。恒瑞医药的转化医学部门也建立了体外类器官培养,实现在模拟的人体器官及肿瘤微环境中进行药物研究。
结 语
类器官技术在新药研发领域未来的应用前景十分广阔,但也存在一些挑战和难点。
其中,最主要的问题是如何制备出高质量的器官模型,这需要对细胞的生物学和生理学过程有更深入的了解,并需要不断改进和优化制备过程。此外,还需要加强法规和伦理的规范和管理。
总之,类器官技术作为新药研发领域的重要工具之一,将在未来发挥越来越重要的作用。我们期待着科研人员在这个领域的不断探索和创新,为人类的健康事业做出更大的贡献。
参考资料:
1. https://xueqiu.com/9650090648/249490339
2. https://www.huborganoids.nl/hub-technology/
3. https://www.jiemian.com/article/7888063.html
4. DOI: 10.1038/nrneph.2015.118
5. https://www.roche.com/about/leadership/hans-clevers/
6. https://doi.org/10.1016/j.cell.2016.05.082
7.https://mp.weixin.qq.com/s/3KU4aQom61P–pX0MSrhZw
8. https://www.bio-accurate.com/jishupintai/