2月CDE一致性评价月报
来源:药智网 | 发布时间:2023-03-14
看点
• 2023年2月CDE新增一致性评价受理号120个(72个品种、74家企业)。
• 2023年2月有198个受理号(含视同通过)涉及117个品种过评。
根据药智数据企业版-仿制药一致性评价分析系统显示,2023年2月份新增一致性评价受理号120个,198个受理号(含视同通过受理号131个)过评。(文末附2023年2月申报与过评一致性评价详情表)
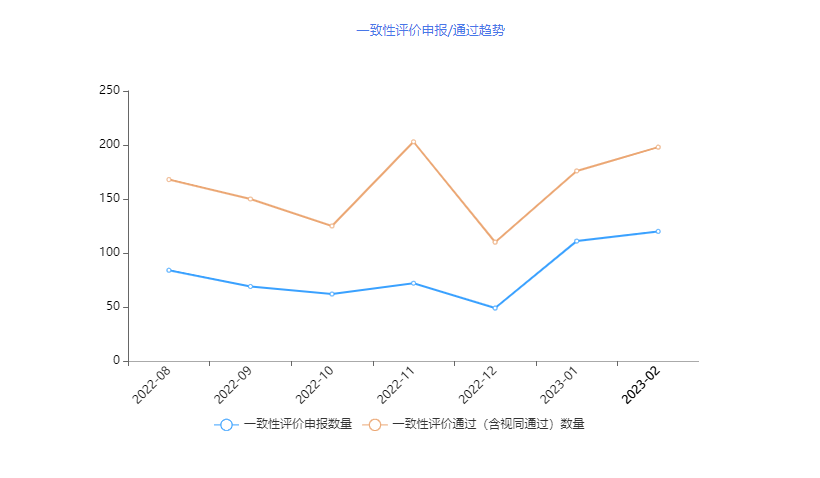
图1 2022年8月-2023年02月申报/通过趋势
图片来源:药智数据
一、过评详情
2023年2月,有67个一致性评价受理号和131个仿制药上市申请受理号视同通过一致性评价,涉及117家企业的126个品种。
其中,由于部分新批准药品还没能收集到详细信息等原因,导致一致性评价数据库中的数据和注册数据可能会存在差异,现在将整理出的2023年2月首家过评的9个药品信息放在表1中,供大家参考。
从过评企业而言,2023年2月上榜企业通过的受理号数量差异不大,河南科伦以6个受理号过评位居榜首,福安庆余堂以5个受理号过评排名第二,成都倍特、海南通用三洋、福抗药业、苏州中化以4个受理号过评并列第三。详情见下图
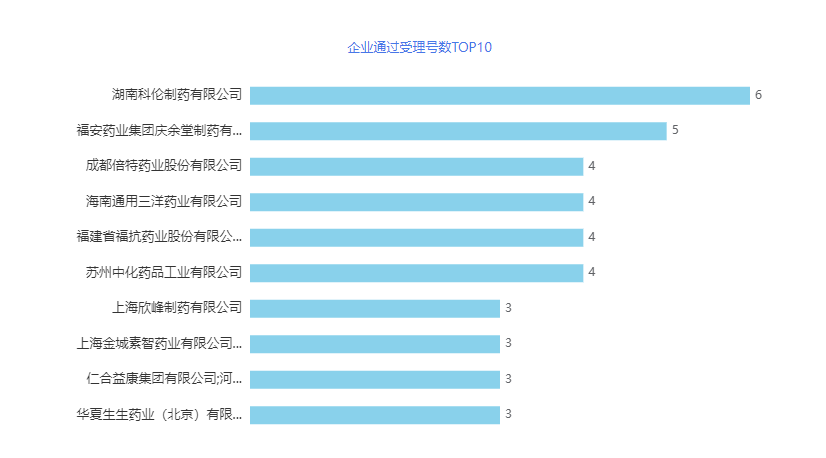
图2 2023年02月企业通过受理号数TOP10
图片来源:药智数据
湖南科伦制药有限公司拥有大容量注射剂、胶囊剂、片剂、颗粒剂、粉针剂、喷雾剂、小容量注射剂等九大剂型的中西药产品,是中南地区药品剂型、品种齐全的综合性制药企业。
公司在2月有4个品种通过/视同通过一致性评价,其中注射用阿莫西林钠克拉维酸钾、注射用头孢哌酮钠舒巴坦钠通过一致性评级补充申请,泊沙康唑口服混悬液和盐酸莫西沙星氯化钠注射液视同通过一致性评价;
公司已有16个品种通过一致性评价、18个品种视同通过一致性评价,还有19个品种的一致性补充申请或仿制药上市申请正在受理中。
福安药业庆余堂制药有限公司经营范围包括:生产小容量注射剂、大容量注射剂、粉针剂(含头孢菌素类)、片剂(含抗肿瘤类)、硬胶囊剂(含抗肿瘤类)、颗粒剂、散剂、吸入溶液剂,粉针剂(青霉素类)、小容量注射剂(提取)等。
公司在2月有注射用头孢哌酮钠舒巴坦钠和注射用美罗培南两个通过/视同通过一致性评价,目前公司已有12个品种通过/视同通过一致性评价,还有10个品种一致性补充申请或仿制药上市申请正在受理中。
从品种看,2023年2月他达拉非片有6家企业过评位居榜首。详情见下图
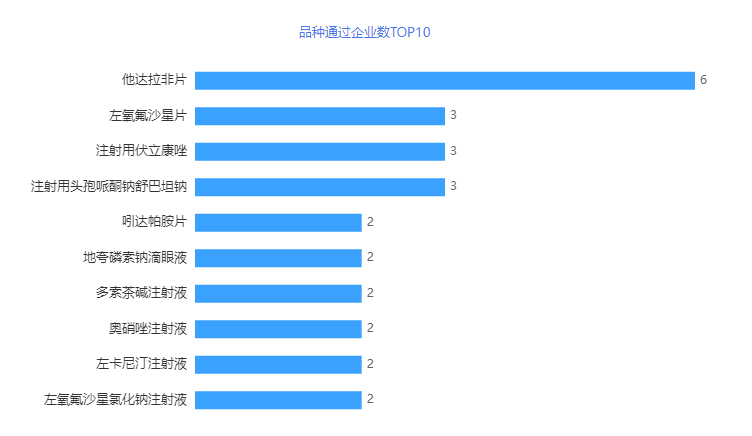
图3 2023年2月品种通过受理号数TOP10
图片来源:药智数据
他达拉非片可用于治疗男性勃起功能障碍和肺动脉高压,处方非医保药品,不能用于女性。
2月获批的6家企业均为仿制药上市申请视同通过一致性评价,分别为:上海汇伦江苏药业有限公司、海南卓力制药有限公司、上海汇伦江苏药业有限公司、江西药都仁和制药有限公司、湖南九典制药股份有限公司、江苏联环药业股份有限公司、扬子江药业集团四川海蓉药业有限公司。
他达拉非片现在已有30家企业的4个规格视同通过一致性评价,目前还有26家企业正在申请上市并被受理。
二、56个品种申报,注射剂占四分之三
2023年2月,CDE新增一致性评价受理号120个,涉及74家企业的72个品种,其中注射剂申报过半,片剂申报超过四分之一。
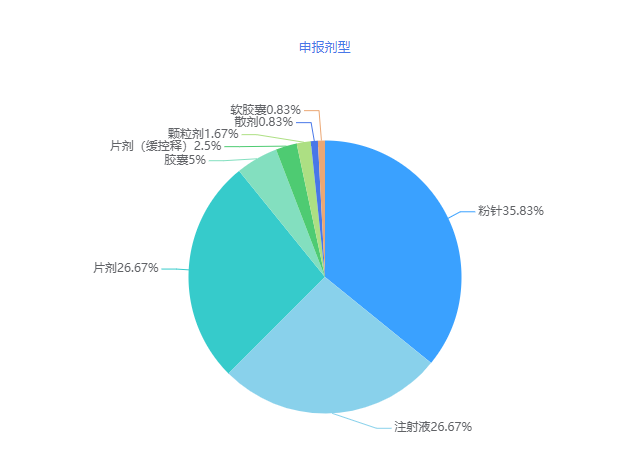
图4 2023年2月申报剂型详情
图片来源:药智数据
申报品种而言,2023年2月,注射用头孢呋辛钠新增15个受理号,遥遥领先于替米沙坦片和注射用头孢曲松钠的5个受理号,成为当之无愧的NO.1。详情见下图。
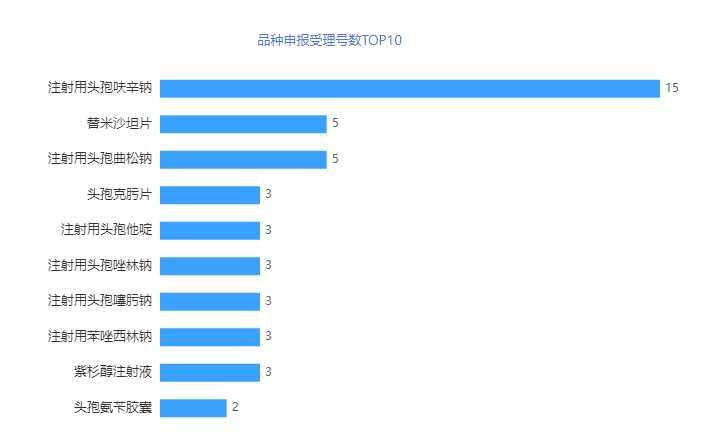
图5 2023年2月品种申报受理号数TOP10
图片来源:药智数据
注射用头孢呋辛钠为广谱的第二代头孢菌素,其作用机理是通过结合细菌蛋白,从而抑制细菌细胞壁的合成。适用于未确定的细菌感染,或敏感细菌引起的感染,还可用于预防各种手术后的感染。
2月,申报受理号数量最多的注射用头孢呋辛钠同时也是2月申报厂家数最多的品种,共5个企业申报,均为一致性评级补充申请,申报企业分别为:安徽省先锋制药有限公司(4个受理号)、海口市制药厂有限公司、石药集团中诺药业(石家庄)有限公司、浙江永宁药业股份有限公司和深圳信立泰药业股份有限公司。
注射用头孢呋辛钠目前已有15家企业过评一致性,还有14家企业已经申报一致性补充申请,并获得受理。
从企业角度,2023年2月安徽省先锋制药有限公司以12个受理号的差距遥遥领先于瑞阳制药股份有限公司和芜湖道润药业有限公司,成为2023年2月企业申报受理号数的第一名。详情见下图
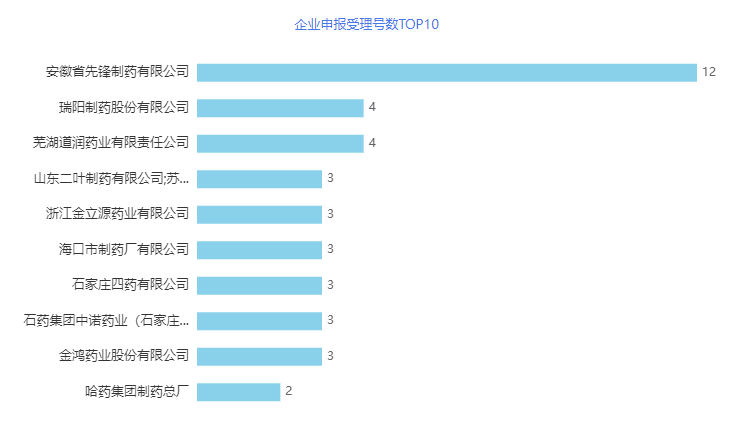
图6 2023年2月企业申报受理号数TOP10
图片来源:药智数据
安徽省先锋制药有限公司成立于2002年8月,已通过国家GMP认证,主要生产头孢类粉针、冻干粉针、普通粉针、胶囊剂、片剂、颗粒剂、化学原料药等类产品。
2月,公司申报了4个品种共12个一致性补充申请受理号,分别为注射用头孢呋辛钠(4个)、注射用头孢唑林钠(3个)、注射用头孢曲松钠(3个)、注射用头孢西丁钠(2个)。
附表1:2023年2月首家通过一致性评价详情表
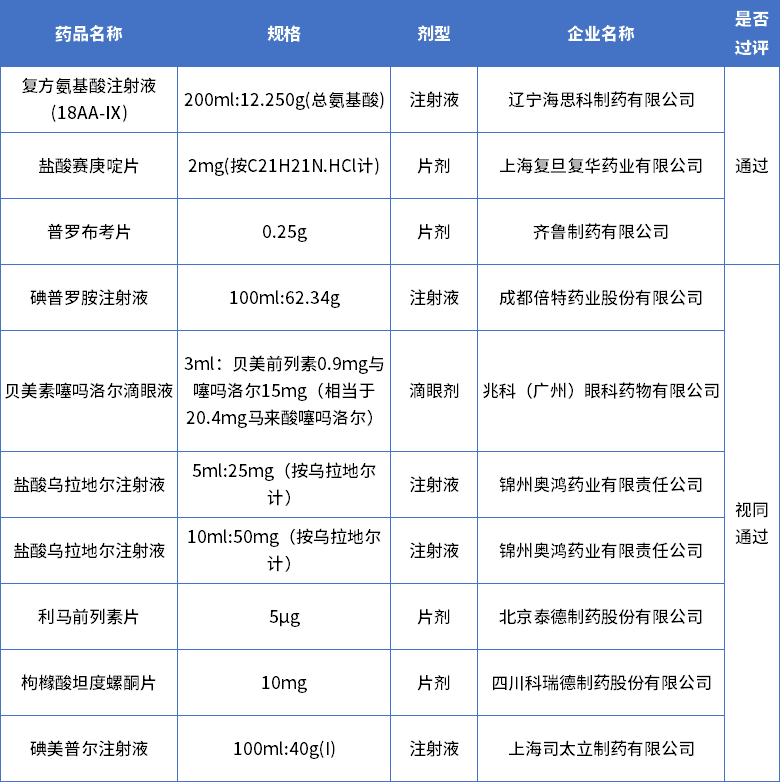
附表2:2023年2月通过(含视同通过)一致性评价详情表
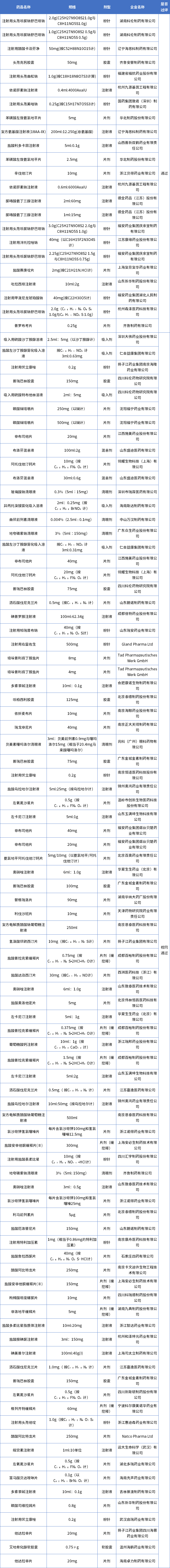
附表3:2023年2月申报一致性评价详情表

数据来源:药智数据
数据截至2023年2月28日