创新药的焦虑时刻:3成初创药企股价破发、近百个临床项目围剿热门靶点
来源:每经网 | 发布时间:2021-04-29
“你们现在投资PD-1还没上市的,会担心这些投资能不能有合理的回报吗?”3月26日,信达生物董事长俞德超在2021红杉全球医疗健康产业峰会分享时,看到国内还有几十个与抗癌广谱药PD-1有关的临床研究,忍不住向台下的投资人发出“灵魂”拷问。
有目共睹,PD-1的竞争已经相当激烈,4个国产PD-1上市不到3年已平均降价80%,而且竞争会越来越激烈,目前国内市场有8个PD-1/L1获批,还有20多个企业的80多个临床在研,而这只是国创新药赛道拥挤的冰山一角。
《每日经济新闻》记者统计发现,部分热门靶点的临床项目数量超过100个。因为竞争过于激烈,部分研发进度不达预期、产品前景生变的创新药企业,也在上市后被资本抛弃。在港交所与科创板上市的43家公司(同时在两地上市的公司只算一家)里,已有16家股价破发,占比超过3成。
俞德超说,高水平重复是国内创新药当下的严峻问题,这是每一个人都要思考的问题。
市场现状:年度“销冠”PD-1也焦虑
俞德超提供的数据显示,2018年~2020年,中国PD(x)-1市场增速为246%,2020年市场规模超过15亿美元,为全球的1/20,预计峰值可能不到80亿美元。
恒瑞医药去年销售收入份额最大,年销售30.69万瓶,业内估计恒瑞PD-1去年收入可能在40亿元上下,与其他3个国产PD-1收入之和相当。
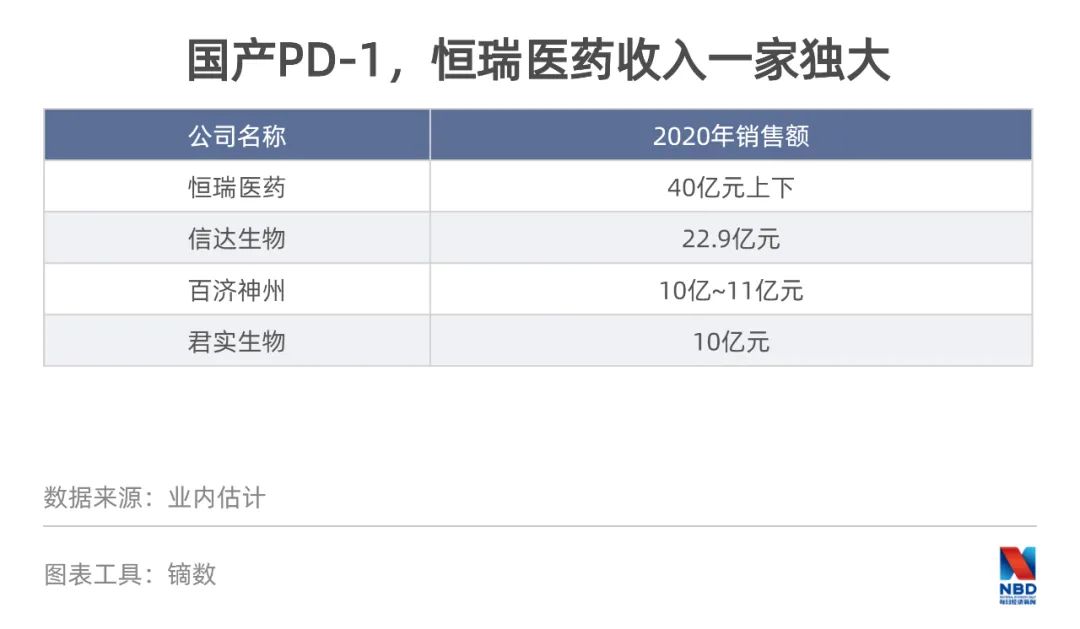
但市场并没因此欣喜,此前业内普遍对抗癌广谱药PD-1的市场规模有着美好设想,甚至有人在第一款产品上市时高喊千亿规模,但两年后,等来的却是缩水50%。
“我们做过对PD-1市场的评估,但显然赶不上政策(变化)。”深圳森瑞投资管理有限公司研究总监何山对《每日经济新闻》记者表示,以前模型测算国内PD-1市场有500亿规模,现在估计腰斩,以后会更小。
西南证券杜向阳团队认为,以PD-1的完整年度年用药金额(医保谈判后为6万元)计算,国内PD-1总市场空间为305亿元;如果PD-1的价格下降到完整年度3万元,则相应渗透率有望提升,预计市场规模可能会收缩到236亿元。
虽然毛利率曾经接近90%,但现在国产PD-1已经开始进入“微利时代”。俞德超指出,医保谈判和控费政策导致中国PD(x)-1价格不到全球水平的1/20,大大降低药企研发的投资回报率。另外,国内研发的同质化竞争也增加了创新药的开发和销售压力。除了已经上市的产品,现在国内批准的PD-1临床项目已经有80多个。
据杜向阳团队预计,未来2年~3年,全球上市PD-1产品将可能超过20个,国内上市的PD-1产品将达到15个,市场竞争日趋激烈。
何山指出,现在PD-1对药企只是“门票”,能帮助其他肿瘤药进入科室,价格竞争下肿瘤管线多的药企还好,必须咬牙做,但本身肿瘤科资源不多的就会越做越亏。而大药企选择开发PD-1管线,主要还是希望把“门票”掌握在自己手中。
俞德超提到,2020年中国癌症新发病例数约为457万例,是全球癌症患者最多的国家(占比23.7%),未满足临床需求很大。现在面临行业同质化竞争和医保控费的双重挑战,还是要聚焦于真创新,并给真正做创新药的企业合理的回报。
实际上,过去半年已经有企业“撤退”。2020年底以来,默沙东、百时美施贵宝、阿斯利康和罗氏均爆出在国外撤销PD-1/L1产品适应症的消息。其中,K药和O药都撤销了小细胞肺癌的适应症,罗氏的T药撤销了尿路上皮癌适应症。今年3月,百奥泰宣布终止了BAT1306(PD-1)的开发。
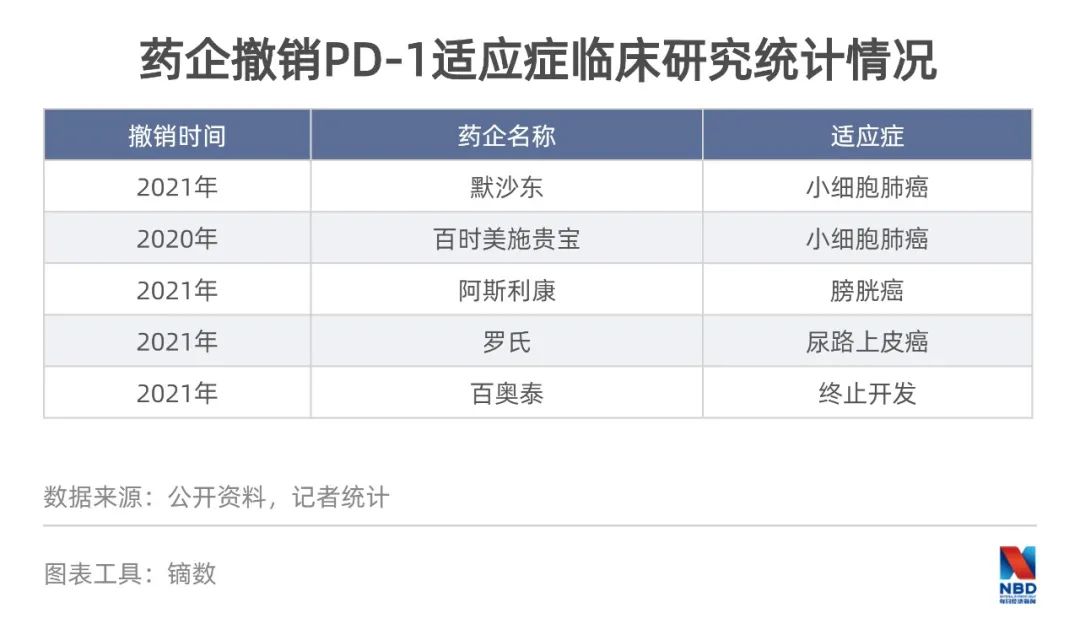
还有些企业,选择以合作的方式在PD-1赛道上进行突围。今年4月,阿斯利康获得君实生物“特瑞普利单抗”在中国大陆非核心市场的推广权及尿路上皮癌适应症的全国独家推广权。
阿斯利康全球执行副总裁王磊在接受《每日经济新闻》记者采访时表示,阿斯利康负责的“特瑞普利单抗”市场主要是中国的四五线及以下县域市场。选择与君实合作,是因为自身的“英飞凡(度伐利尤单抗注射液)”的适应症还较少,联合君实的获批适应症有望加强在临床上的竞争力。
但PD-1的白热化竞争还没有到头。GBI Health药监数据显示,除获批的8个PD-1/L1,临床审批已通过的PD-1有48个企业,涉及受理号361条。其中进口企业有10家,国产企业有38家。
研发之路:仿创扎堆,“自主创新不等于自己创新”
为什么自带“创新药”属性的药企都要开发PD-1?一方面与中国药物生态环境有很大关系。2010年以前,中国新药可及性低,更难进入医保目录,患者经济负担大,所以先进药物的渗透率远低于全球平均水平。
进入2010年后,一大批具备海外留学和跨国药企工作背景的人才回流创业,他们清楚中国新药上市和可及性与发达国家的差距,所以倾向于选国外尚未上市,但已经处于二、三期临床阶段的创新药,尝试同类靶点产品研发。这类研发项目被称为快速跟随(fast follow)仿创,药物研发风险较首创更低,还有更多经验可以借鉴。
另一方面,PD-1可能会成为肿瘤治疗的基石药物。百奥泰总经理李胜峰近日对外表示,不久的将来PD-1或会成为基础性用药,未来谈起PD-1或许就像讨论抗生素一样稀松平常。
但国内自主研发的创新药还处于“补缺”、“跟随”状态。《每日经济新闻》记者统计发现,2018年~2020年,国内共批准33个1类新药上市,包含PD-1、恩沙替尼、奥美替尼、氟马替尼等重磅创新药品,但绝大多数还是快速仿创。比如,恒瑞医药新药“甲苯磺酸瑞马唑仑”是在老药“瑞马唑仑”基础上开发出的甲苯磺酸盐类化合物,“瑞马唑仑”原研药为英国的CeNeS;豪森药业获批的“甲磺酸氟马替尼”是第二代TKI抑制剂药物,结构上被认为是升级版的“格列卫”。
另有数据显示,全球前十大创新药热门靶点的集中度为13.08%,国内达到29.28%,最拥挤的靶点VEGFR/VEGF、EGFR、PD-1/PD-L1等靶点的在研项目,中国的研发数量分别为98个、89个和69个,在全球同靶点中占比均超过50%。
繁华背后,中金资本运营有限公司总裁单俊葆喊出:“自主创新不等于自己创新。”俞德超也强调,高水平重复是一个非常严峻的问题,每个人都要思考接下来国内创新药要怎么走。两年前,信达生物做了一个比较大的决定,今后发展基于“创新+全球化”两方面,开发具有全球first-in-class潜力的药物,在全球市场开发和商业化信达的药物。
科越医药首席业务官何奇志在谈到药企扎堆仿创现象时也谈到,应该注意到fast follow的现象,但不应该担心它,“企业扎堆fast follow跟我们这个行业还处在比较早期,不是特别成熟有关。我们的人才、资本都还处于早期,企业不敢冒太大风险,因为一旦风险太高就怕自己出局了”。
何奇志进一步表示,fast follow就像是较低的好摘的“果子”,走在前面的先发现的人把“果子”摘下来了,后面的人还想去摘,却发现果子已经没有了,这就会让投资人、企业面临一些风险与问题,所以大家还是要往差异化的方向去走,但这就要做好“打大仗”的准备。
Fast follow成药性高,扎堆上市意味着患者能以更低的价格接触到更多用药选择。但对于药企而言,或将在更短时间内面临大量同质化产品抢夺存量市场的局面,进一步导致“价格战”避无可避。
百济神州总裁吴晓滨近日公开表示,他觉得可能还是生产同类药品的企业太多,三家很良性、五家也很良性,几十家就开始拼搏了,这可能会打破很多规矩。
《每日经济新闻》记者研究发现,在上市产品普遍不超过5个的当下,如果主打产品不属于first-in-class,处境就会相对尴尬,既要面对原研产品降价,还要面临国产同质化竞争,如果商业化能力不足,利润甚至无法覆盖巨额的研发支出。
此前在跨国药企任要职多年的吴晓滨认为,商业化能力对创新药企来说非常重要,恒瑞是我国从传统企业转变成创新企业最成功的案例。恒瑞不需要证明它的商业化能力,要证明它的创新能力。而biotech公司恰恰相反,能不能走好商业化之路?能不能做好制造?这是非常重要的大考。
高特佳投资集团执行合伙人王海蛟公开谈到,同类抗癌药的同一个靶点药,第一个上市的产品能够占到销售收入的40%~50%,第二个只能拿到销售额的20%~30%,第三个可能只能拿到第二名的一半,第4名、第5名就基本上不具有投资价值了。此外,即便新上市能够提供较大的先发优势,然而,小公司在营销上会处于相对弱势。
商业化能力恰好是很多初创药企的短板。再鼎医药创始人、董事长杜莹出席2021红杉全球医疗健康产业峰会时坦言,传统的医药公司销售能力很强,销售可以铺到四线五线城市,在国内也有这些经验。而像再鼎医药这类公司就并不懂怎么卖药,“我们只是搞研发的”。
据《每日经济新闻》记者统计,信达生物、百济神州的销售团队规模均在千人以上,君实生物为912人左右,百奥泰260人,而恒瑞医药肿瘤线销售人员超过6000名,PD-1专职销售人员接近2000人。还有一些尚无产品上市的biotech,甚至没有组建销售团队。
股价表现:3成未盈利创新药企业破发
过去5年,国内生物医药如沐春风。俞德超也在2021红杉全球医疗健康产业峰会上感慨,过去5年是中国医药创新研发最好的5年,每年新药审批数量已经接近FDA的速度,进入美国、欧洲临床研究的数量也在过去5年翻了10倍。
药是医生的武器,病人的希望,也是投资人眼里的富矿。特别是港股18A及科创板新规实施后,两地对上市企业盈利数据没有明确要求,对于大量尚未实现盈利的创新药企业而言,资本市场是融资的优先选项。据《每日经济新闻》记者统计,截至4月27日,共有26家创新药企业在港交所上市、17家在科创板上市。
因为研发投入大,初创药企普遍亏损,在上市前基本经过4轮以上融资。但作为公众公司登陆资本市场后,这些公司就要面对市场投资者的抉择。显然,有些公司已经不像上市前那样受资本青睐,有16家股价破发,其中港交所12家、科创板4家。
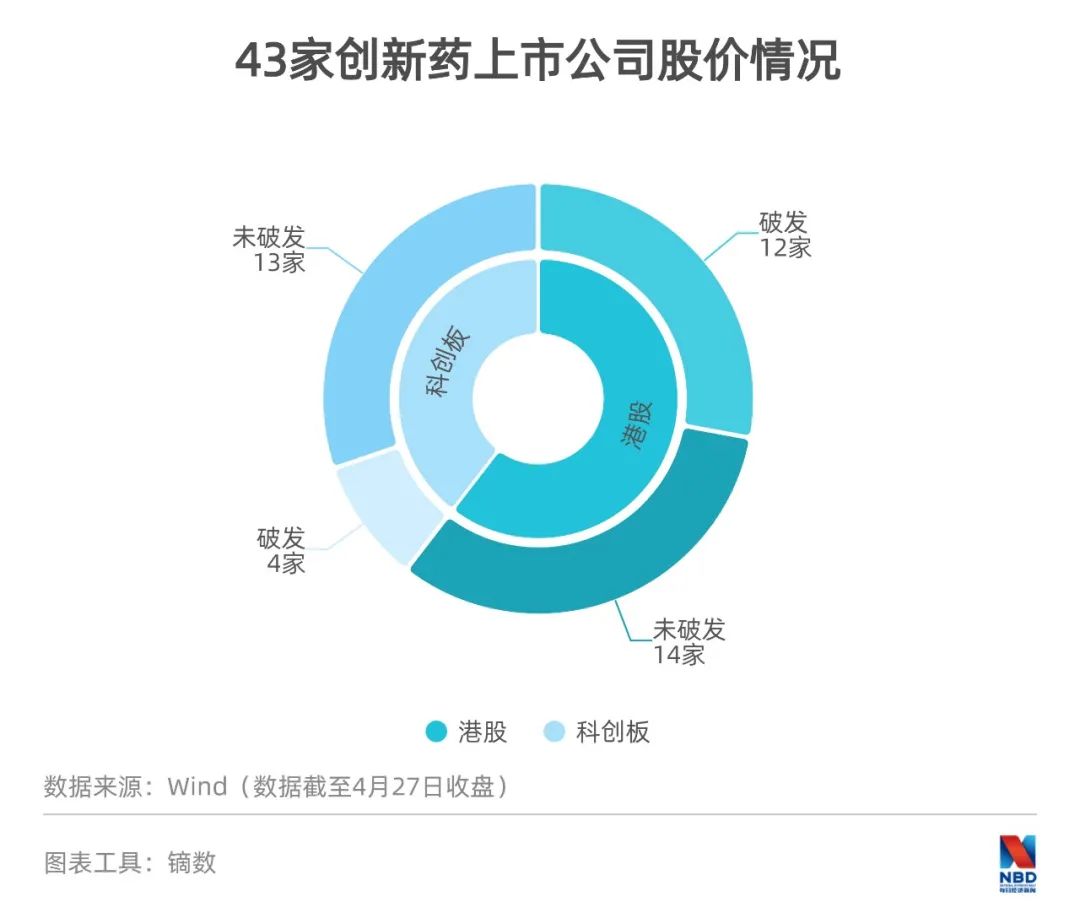
而去年上市的12家企业,也有不少出现过破发的情况。其中,和铂医药和药明巨诺IPO当天破发;加科思和德琪医药在上市3天后破发;开拓药业、嘉和生物、永泰生物也在上市后的短短时间内跌破发行价。
作为适用于18A规定的生物医药企业,歌礼制药-B的发行价定于14港元/股,而截至4月27日收盘时,歌礼制药只有2.87港元/股,缩水80%,可谓被按在地上摩擦,在所有非盈利生物医药企业里跌幅最大。
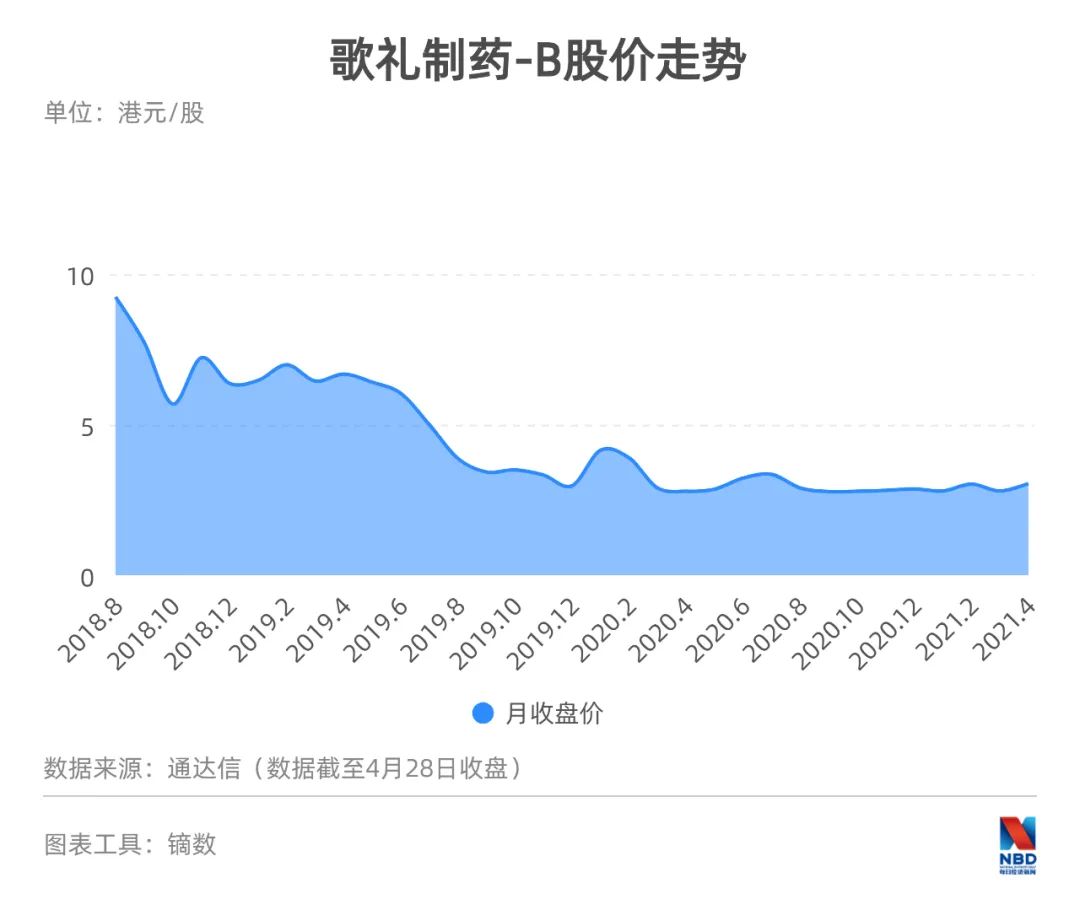
《每日经济新闻》记者了解到,如此不受市场待见与歌礼制药基本面发生变化有很大关系,据其公布的2020年全年业绩,歌礼制药实现营收3500万元,同比下降79.8%。歌礼制药营收主要来自丙肝治疗药物“戈诺卫”,由于新疗法的出现,“戈诺卫”逐渐失去竞争力,导致公司营收大幅下降。
有企业则是因为创新成色不足,让投资者失去兴趣。
百奥泰就是其一。2019年10月,百奥泰首个产品阿达木单抗生物类似药“格乐立”获批,但原研药“修美乐”降价83%进入国家医保目录,“格乐立”定价只比“修美乐”低10%,而且还要同时与信达生物、海正药业、复宏汉霖的生物类似药竞争。
三生国健主打产品“益赛普”是国内风湿病领域首个上市的肿瘤坏死因子(TNF-α)抑制剂,但仍在创新药和生物类似药市场面临多方面的竞争。截至2020年底,国内获批上市的TNF-α抑制剂药物已经超过10个,且在研产品竞争也较为激烈。
另外,作为港交所18A第一股,歌礼制药的丙肝药“达诺瑞韦”的数据并不逊于进口产品,但产品刚刚上市就面临吉利德、默沙东、艾伯维等外资“围剿”。2019年底在医保谈判上的铩羽而归成为“压倒”歌礼的一根稻草。此后连续两年的销售额都不甚理想,虽然手握大笔现金,但奈何后续研发颇为乏力。
嘉和生物虽然在研管线中不乏PD-1、TNF-a、VEGF、CD20等热门靶点,但根据其目前产品进展,基本上很难在上市速度上成为国产前三,失去市场先机的同时也会面临更激烈的价格战,甚至是生物药集采。
还有些公司则面临主打产品专利即将到期的危机。作为前沿生物的核心产品,艾可宁是中国首个治疗艾滋病的原创新药、全球首个长效HIV融合抑制剂,但艾可宁能否在2023年核心专利到期前获得新专利的保护,存在不确定性。一旦得不到新专利的保护,市场将不可避免地出现仿制药。
而在2020年上市的公司里,未破发的分别为欧康维视、康方生物、诺诚健华、荣昌生物和云顶新耀。除康方生物外,其他4家企业均有核心产品处于上市/NDA(申请新药上市)阶段。
多位医药投资人士表示,机构对未盈利公司的估值,主要基于在研产品线的潜力以及对未来的预期,一旦在研项目遇到困难或者失败,往往会引起股价的大幅波动,给投资者带来负面影响。另外,研发进度缓慢、没有竞争优势,也会被资本所抛弃。
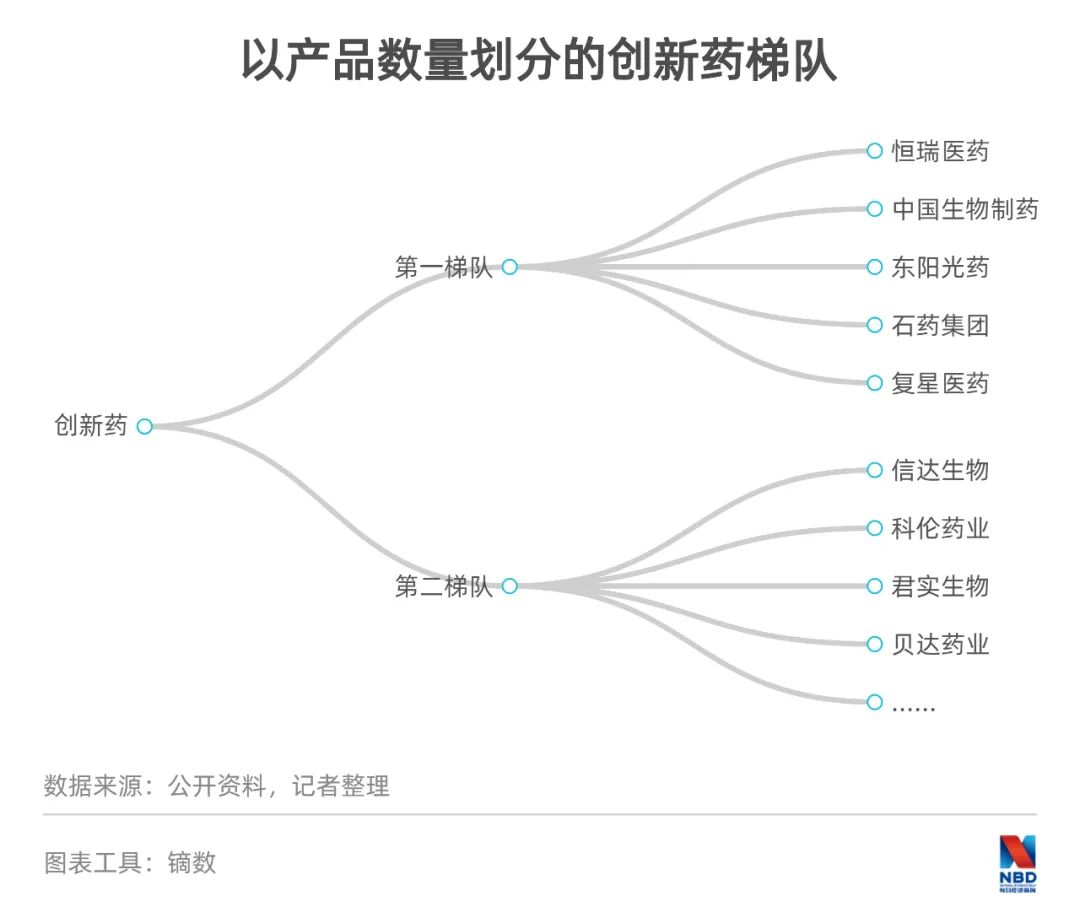
医药上市企业、尤其是创新药企业的股价表现,与企业的研发成色息息相关。相关数据显示,以数量计,创新药第一梯队有5家企业,分别是恒瑞医药、中国生物制药、东阳光药、石药集团和复星医药,这5家企业均有10个以上创新药;第二梯队包括信达生物、科伦药业、君实生物、贝达药业等18家企业,均有5个以上创新药。第一和第二梯队企业分别拥有100个和107个创新药,合计占到创新药总数的34%。
有市场人士表示,随着市场的成熟,创新药企业一定会出现两极分化:有创新能力、研发能力、产品过硬的企业会受到投资人追捧,股价持续上涨;反之,无创新、研发能力落后、没有特色的企业可能会出现发行失败、破发、交易量(市值)低迷的情况,甚至退市。
企业选择:或布局创新性靶点,也有断臂求生的
行业龙头高呼过度竞争,上市公司股价接连破发,创新药不香了吗?《每日经济新闻》记者深入研究发现,虽然生物医药行业景气度高,初创型公司能快速获得资本“输血”和上市,但市场评判公司的标准没有变,还是看在研产品线的进展,在大部分企业扎堆到同一研发项目后,就是比谁更快、有效率更高。
“如果不在第一梯队,就算是热门产品,也等于失去了抢占市场的机会,还可能上市后面临集采,或者价格战,这些初创企业的商业化能力几乎是空白,面临的挑战不小。”一位长期关注医药行业的专业投资人士对记者表示,很多破发的生物医药公司都是这种情况。
在4月22日召开的一场会议上,百济神州全球总裁吴晓滨在会议上公开表示,我国的医药创新大部分还集中在迭代阶段,first-in-class还比较少。
会后,阿斯利康全球执行副总裁王磊也表示,first-in-class是基础科学的突破,只有基础科学做好了,才有资格去做first-in-class。“first-in-class有偶然性,既要有运气又要有基础科学的积累。现在大部分的创新医药企业其实更适合做迭代创新,我觉得做迭代创新也不应该觉得羞耻,因为很多产业都是靠做迭代创新起来的。”王磊称。
王磊强调,做迭代创新关键得沉得住气,一年一年忍受投入资金、人力,忍受痛苦和挫折,创新可能从迭代中演化出来了。
值得注意的是,越来越多“中国制造”出现在全球创新药圈层。2018年以前,中国创新药每年license-out的交易量几乎不超过5个,而自2018年起,这一数字开始攀升。到2020年,据不完全统计,中国创新药license-out的数量已经翻了两番,达到24个。其中,天境生物与艾伯维高达30亿美元的交易合作,便刷新了中国创新药license-out的交易纪录,成为新药BD领域当之无愧的重磅。
俞德超也表示,中国创新的标准应该是全球化创新的标准,中国新药面向的市场应该是全球化的市场。
“近几年医疗行业发展迅速,有点像2001年时的PC互联网和2010年的移动互联网,但也还有很长的路要走。”在2021红杉全球医疗健康产业峰会上,红杉资本全球执行合伙人、红杉资本中国基金创始及执行合伙人沈南鹏说,尽量不要成为一家仿创公司,而是要成为一家“first-in-class”企业。这是他在优秀的TMT和医疗领域创业者身上看到的共同品质。这些创业者往往也非常有韧性,他们都着眼于创造百年企业,而他们也是能够笑到最后的人。
沈南鹏表示,在过去的一到两年里,人工智能在新药开发领域里出现了多个平台型的突破。“我们看到一个交叉点正在兴旺地发展,就是IT和BT,其融合速度超过历史上任何时刻。从我们一直比较关注的网上医疗服务,再到AI在诊断、治疗全流程服务中的应用,在新药开发中的应用,这些都构成了整个医疗行业新的革命。”
记者手记丨创新药市场仍在“等风来”
如果将仿创药比作低处的“果子”,因为其易得——成本低、风险小,树下的人自然都渴望摘到这些“果子”。但有人造梯、有人织网,速度有快有慢,当前面的人将“果子”摘了,后面想摘的就发现没有了,而已经花在路上的时间、金钱,就是后来者要付出的代价。
这就是多位创新药企人士所担心的,仿创药研发扎堆后暴露在药企和投资人面前的问题。
PD-1的案例只是我国创新药现状的一个缩影,从“香饽饽”变成打价格战的红海,市场的变化远比研发一款新药来得快。投资人开始担心有没有合理回报,厂家们也在担心以“十年时间、十亿投资”换来的新药最后能分得多大的“蛋糕”。
但对企业而言,做fast-follow还是first-in-class是硬币的两面。First-in-class这一面是哥伦布航海式的探险,可能寻获新大陆,但也有可能葬身深海。
或许,国内的创新药市场还在等待成熟,等待基础科学的进步、资本真正支持自主创新,还有创新药企们有更大的勇气和更雄厚的底气去征服没有人登顶过的高山。