2019年度FDA批准的首仿药总结
来源:新浪新闻 | 发布时间:2020-01-10
摘要:FDA的药物评估和研究中心对其在2019年批准的首仿药进行了总结。2019年,FDA共计批准108个首仿药,涉及53个制药公司。
2020年1月8日,FDA的药物评估和研究中心(CDER)对其在2019年批准的首仿药(First-Time Generic Drug)进行了总结。
CDER每年都会批准各种新药产品。对于仿制药,FDA提供了将安全、有效、高质量的科学和法规建议,确保将这些通用替代品推向市场,满足所需,为患者提供了更多可负担的治疗选择。
“首仿药”——正如其名字所表示的——这是FDA首次批准、允许制造商在美国销售非专利药产品。FDA认为首仿药对公共健康很重要,并优先审查这些呈件。
2019年,FDA共计批准108个首仿药,涉及53个制药公司。
获批品种数量最多的前六家药企为:
梯瓦制药 Teva Pharmaceuticals(以色列) 11个
迈兰制药 Mylan Pharmaceuticals(美国) 9个
阿姆尼尔制药 Amneal Pharmaceuticals(美国) 7个
帕尔制药 Par Pharmaceutical(美国) 6个
太阳制药 Sun Pharmaceutical(印度) 4个
Novitium 制药 Novitium Pharma(美国) 4个
.png)
首仿药获批公司完整清单请扫描文后二维码查看。
按照品种计算,共计69个品种获得首仿的批准。获批次数最多的前五个首仿药是:
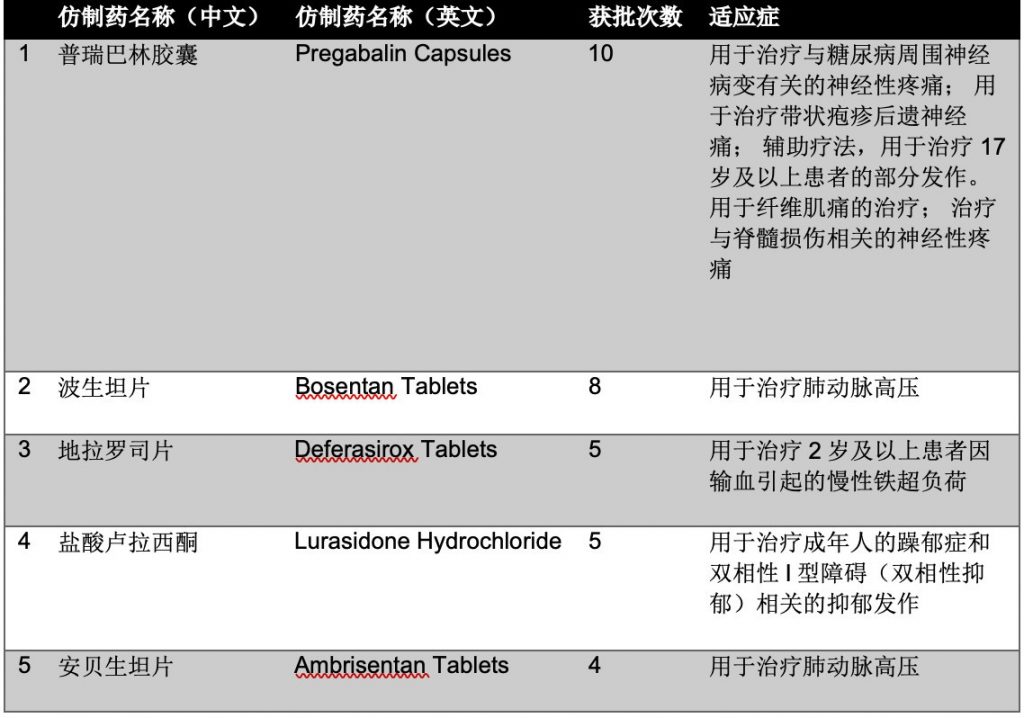
首仿药获批品种完整清单请扫描文后二维码查看。
扫码查看更多详情
