CAR-T、TCR-T细胞技术的当前挑战和未来方向
来源:生物制品圈 | 发布时间:2023-08-03
摘要:在过去几年中,过继细胞疗法(ACT)作为一种新疗法,在肿瘤免疫管线中的地位逐步上升。这在很大程度上是由于最近批准的嵌合抗原受体(CAR)-T细胞疗法及其对某些可溶性肿瘤的显着疗效。ACT的一大焦点在于T细胞以及如何对其进行基因修饰以靶向并杀死肿瘤细胞。目前使用的基因修饰T细胞要么配备了工程化的CAR,要么配备了T细胞受体(TCR)。这两种策略各有优缺点。虽然CAR-T细胞疗法已经用于临床,但这些疗法在治疗实体瘤时面临挑战。新设计的下一代CAR-T细胞或许能够克服这些障碍。此外,CAR仅限于表面抗原。靶向细胞内抗原的基因工程TCR-T细胞可能为实体瘤的治疗提供必要的品质。本文将对CAR-T和TCR-T细胞技术的主要进展进行综述。此外,我们将涵盖正在进行的临床试验,讨论当前存在的挑战,并提供该领域未来方向的评估。
引言
癌症免疫疗法,特别是免疫检查点抑制(ICI),在治疗越来越多的癌症实体中显示出高效率。然而,很大一部分患者对ICI没有反应,这些患者对替代治疗方案的医疗需求未得到满足。一个有希望的治疗难治性肿瘤的新途径是过继T细胞治疗领域,目前正在进行数百项临床试验。这种基于细胞的个性化治疗要么利用患者自身的肿瘤浸润淋巴细胞(TIL),要么使用带有工程嵌合抗原受体(CAR)或T细胞受体(TCR)的转基因T细胞来靶向和杀死肿瘤细胞。其最突出的形式是CAR-T细胞疗法,它在某些血液病中显示出巨大的疗效,并且几种CAR- T细胞疗法已经被美国食品药品管理局(FDA)批准用于治疗血癌。CAR设计在短时间内经历了多次迭代,与前几代CAR形式相比取得了令人印象深刻的改进。然而,到目前为止,它们在治疗实体瘤方面的效果有限。另一方面,TCR-T细胞疗法尚未被批准用于临床应用,但目前正在进行早期临床试验。与CAR-T细胞相比,TCR-T细胞不局限于表面抗原,对肿瘤细胞上的抗原水平更为敏感。然而,它们依赖于患者的特定人类白细胞抗原(HLA)组成,限制了这种治疗的特定患者群体。在这里,我们将概述CAR-T和TCR-T细胞治疗的广阔领域,从制造过程及其对T细胞产品抗肿瘤活性的影响到改善难治性肿瘤治疗的潜在策略的可行性。
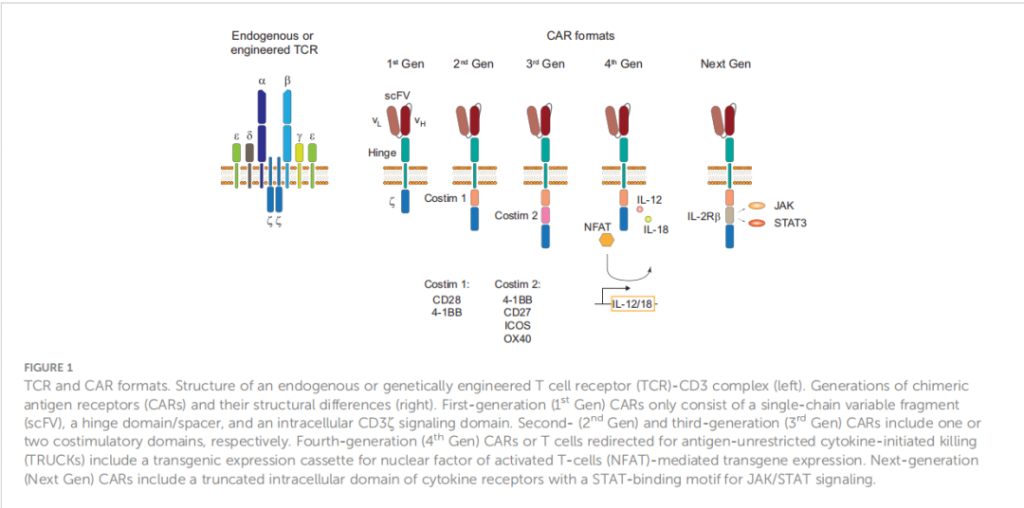
图1 TCR和CAR形式。内源性或基因工程T细胞受体(TCR)-CD3复合物的结构(左)。嵌合抗原受体(CARs)的代次及其结构差异(右)。第一代CAR仅由单链可变片段(scFV)、铰链结构域/间隔区和细胞内CD3ζ信号传导结构域组成。第二代和第三代CAR分别包括一个或两个共刺激域。第四代CAR或T细胞重定向用于抗原不受限制的细胞因子启动杀伤(TRUCK)包括一个转基因表达盒,用于活化T细胞核因子(NFAT)介导的转基因表达。下一代CAR包括一个截断的细胞因子受体胞内结构域,具有STAT结合基序,用于JAK/STAT信号传导。
工程化CAR和TCR形式的设计
内源性和工程化的TCR识别靶细胞上代表感兴趣抗原的肽- HLA复合物。工程TCR通常不会偏离α/β链异源二聚体的经典TCR结构,并且能够形成功能性TCR- CD3复合物(图1,左)。在抗原识别后,两个细胞内CD3ζ结构域诱导下游TCR信号传导。相比之下,CAR被设计成由单链可变片段(scFV)、铰链结构域、跨膜结构域和细胞内共刺激信号域组成的单分子(图1,右)。抗原识别由scFV促进,scFV是抗体轻链和重链可变区域的融合蛋白,通过肽连接子(linker)连接。与工程或内源性TCR相反,CAR不能组装CD3复合物,并且scFV对表面抗原的抗原识别是HLA非依赖的。第一代CAR证明了这一概念的可行性,表明与细胞内CD3ζ结构域的偶联足以在抗原识别时进行下游信号传导。该形式的下一个迭代包括一个靠近膜的共刺激信号域,CD28或4-1BB,以结合初级和共刺激信号,增加IL-2的产生。为了增强抗肿瘤活性并可能增加CAR-T细胞的持续性,在第三代CAR-T细胞中添加了第二个共刺激域。目前在临床研究中测试了许多第三代CAR-T细胞(NCT03676504;NCT04049513)显示出良好的安全性,并将评估其在CD19+恶性肿瘤患者中的持续性。支持这一观点的一个有趣发现来自I期临床试验(NCT01853631),该试验观察到,当同时输注于r/r NHL患者时,CD19第三代(CD28和4-1BB)CAR-T细胞比第二代(CD28)细胞扩增更大,持续时间更长。一个新的概念被应用于第四代CAR或T细胞重定向,用于抗原不受限制的细胞因子启动杀伤(TRUCKs)。TRUCKs将CAR与转基因表达盒结合起来,该表达盒由合成核因子活化T细胞(NFAT)反应元件与IL-2最小启动子和转基因组成。CD3ζ介导的信号最终导致NFAT的磷酸化、易位到细胞核以及转基因的表达。由于TRUCKs概念依赖于CD3ζ介导的NFAT易位,因此它不仅适用于CAR-T细胞,也适用于TCR-T细胞。这种方法中最常见的转基因蛋白是IL-12和IL-18,但目前正在探索许多其他细胞因子和酶。TRUCKs概念对于结合T细胞介导的杀伤和通过分泌细胞因子对肿瘤微环境(TME)的免疫调节来治疗实体肿瘤具有特别的意义。TME中IL-12和IL-18的分泌可能通过吸引和激活巨噬细胞和NK细胞来增强抗肿瘤级联反应。由于CAR构建体没有细胞运动介导信号的特定结构域(也称为信号3),新的发展包括CAR具有细胞因子受体的截断胞内结构域(例如IL-2受体β(IL-2Rβ)结构域)和STAT3结合基元来诱导JAK/STAT信号传导。与第二代CAR-T细胞相比,这种方法在体外阻止了终末分化,并在临床前肿瘤模型中显示出更高的持久性和抗肿瘤活性,但这种形式可能需要进一步评估以证明其转化潜力。与典型T细胞相比,CAR-T细胞固有地具有较低的抗原敏感性,并且强直性CAR信号传导与CAR-T细胞衰竭有关。这可能至少部分是由于含有10个富含酪氨酸的免疫受体激活基序(ITAM)的TCR-CD3复合物与仅含有3个ITAM的传统CAR相比,其信号传导方式存在差异。为了将内源性CD3信号复合物与抗体介导的抗原识别结合起来,已经开发了一种双链嵌合受体,称为合成TCR和抗原受体(STAR),将恒定的α和β结构域融合到抗体的轻链和重链可变区域。经抗原识别,在实体瘤小鼠模型中,与第二代CAR-T细胞相比,STAR已被证明提供TCR样信号,具有优越的抗原敏感性和抗肿瘤活性。这可能是一个有趣的新设计,然而,由于其增强的抗原敏感性而增加靶外肿瘤毒性的潜在风险可能限制其临床应用,需要进行研究。
基因工程T细胞的生产
基因工程T细胞产品最初是在学术机构中常见的开放式自我操作生物反应器中开发的。然而,这些系统需要训练有素的工作人员和严格的卫生监测,以避免污染。因此,随着CAR-T细胞疗法的临床成功,生产不仅在工业设施中,而且在学术机构中越来越多地转向封闭和半自动或全自动平台。CAR-T细胞制造平台的大多数进展,只要对方案进行一些修改,就可能转移到TCR-T细胞的生产中。因此,TCR-T细胞疗法极大地受益于ACT领域的创新,这些创新是由CAR-T细胞疗法的临床批准启动的。CAR-T和TCR-T细胞治疗的一般工作流程如图2所示,本章将对其进行详细总结。
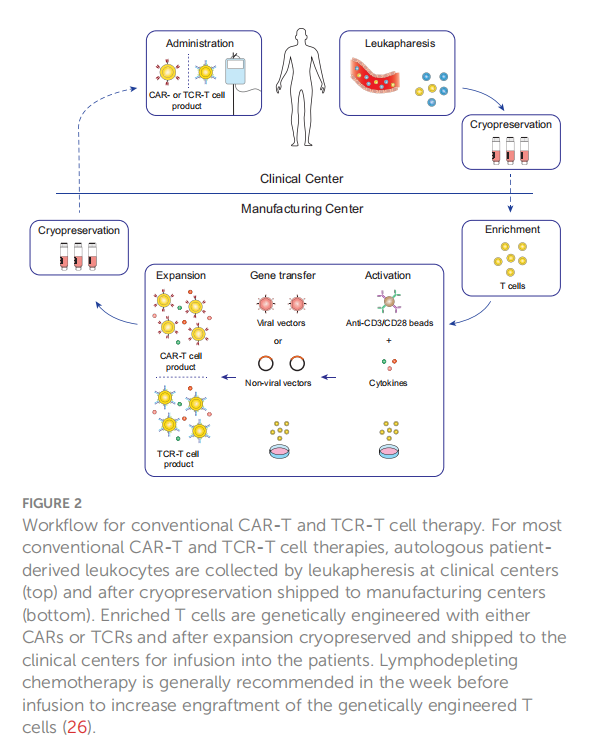
图2 传统CAR-T和TCR-T细胞治疗的工作流程。对于大多数传统的CAR-T和TCR-T细胞疗法,自体患者来源的白细胞是在临床中心(上)通过白细胞分离收集的,冷冻保存后运送到制造中心(下)。富集的T细胞用CAR或TCR进行基因工程改造,扩增后冷冻保存并运送到临床中心输注到患者体内。通常建议在输注前一周进行淋巴消耗化疗,以增加基因工程T细胞的植入。
细胞收集和处理
为了产生基因工程T细胞,白细胞要么从患者(自体)收集,要么从健康供体(异体)收集。值得注意的是,迄今为止,所有FDA批准的CAR-T细胞疗法都是使用患者来源的自体细胞,但也有许多临床试验研究使用供体来源的异体细胞。白细胞分离术是收集白细胞的首选方法,因为它在医疗中心可用,患者耐受性强,而且生产T细胞的产量高。收集的细胞要么以新鲜状态直接用于制造,要么更常见的是冷冻保存以供以后处理。冷冻保存在临床中心或在某些情况下在制造中心进行。尽管低温保存对细胞活力有影响,但现场制造基因工程T细胞通常是不可行的——除了少数学术临床研究(NCT03676504)——而CAR-T细胞的生成可以用冷冻细胞实现。对于不同的T细胞产品,不同的临床和生产中心的冷冻保存程序在冷冻介质组成和持续时间方面存在差异,但它们对最终产品质量的影响尚未得到可比评估。
起始细胞组成对抗肿瘤免疫的影响
起始材料的细胞组成对于成功设计具有长寿命抗肿瘤特性的功能性CAR-T细胞产品至关重要。从白细胞分离产品中富集T细胞可以通过磁分离珠实现,迄今为止所有批准的CAR-T细胞疗法都使用CD4+和CD8+ T细胞在联合或单独培养环境中进行富集。因此,CAR-T细胞疗法不限于产生CD8+ CAR-T细胞反应,而且还利用CD4+ CAR-T细胞以协同方式提高其抗肿瘤反应。与CD8+ T细胞相比,CD4+ T细胞表现出更强的可塑性,由辅助性T细胞(Th)亚群和调节性T细胞(Treg)组成。CD4+亚群的扰动和Treg细胞的产生可能会对临床反应产生影响。在最近的一项研究中,CAR-Treg细胞的扩增与对CD19 CAR-T细胞治疗的耐药性有关。因此,将CD4+ T细胞分化为“最佳”抗肿瘤表型,并在制造过程中限制CAR-Treg细胞的产生,可能对改善ACT至关重要。CD4+和CD8+ T细胞的分离制造和给药已经应用于CD19 CAR-T细胞疗法Breyanzi,以减少CD4+和CD8+ CAR-T细胞组成之间的可变性,并以剂量确定的方式给药。在一项CD22 CAR-T细胞治疗患有CD22+ B细胞肿瘤的儿童和年轻人的临床试验中,将制造方案改为CD4+和CD8+ T细胞选择提高了制造的可行性,降低了变异性,然而,这导致炎症毒性增加,需要降低剂量。总体完全缓解率仍然很高,达到70%,但根据CAR-T细胞产物中CD4+/CD8+细胞的比例,可能表明CAR-T细胞诱导的毒性。在某些情况下,单独制造CD4+和CD8+ CAR-T细胞可能会损害CAR-T细胞的扩增。在第三代CD20 CAR-T细胞疗法中,从CD4+/CD8+选择到联合培养环境的改变提高了制造的可行性和临床反应率。此外,特异性记忆T细胞亚群的富集和分化,如多能T记忆干细胞(TSCM),可能会改善CAR-T细胞的抗肿瘤反应。这可能是由于T细胞具有一定程度的干性,具有更高的T细胞持久性和更少的衰竭易感性。总的来说,制造过程中细胞成分对T细胞治疗抗肿瘤疗效的影响仍需要在未来的临床研究中进行比较。
制造过程中的激活条件
T细胞被激活以进行有效的基因转移和扩增,这通常通过使用抗CD3/CD28顺磁珠进行病毒转导来实现。然而,据报道,这种方法在非富集产物中有利于CD4+ T细胞而不是CD8+ T细胞的扩增,并且在某些情况下可能导致CD8+ T细胞的低效扩增。这可能是由于CD28介导的信号在CD4+ T细胞中的重要性,而4-1BB共刺激对CD8+记忆T细胞的扩张更有利。为了克服这一点,目前的方案除了抗CD3/CD28磁珠外,还引入了细胞因子鸡尾酒来支持扩增,并使分化向具有固有良好抗肿瘤特性的表型倾斜。例如,在标准方案中使用细胞因子IL-2,因为它对T细胞的有丝分裂作用及其在肿瘤免疫背景下对T细胞有效性的潜在益处。此外,在制造过程中刺激的激活条件和强度也可以决定基因工程T细胞在遇到肿瘤细胞上的同源抗原时是否容易衰竭。与抗CD3/CD28磁珠相比,可溶性抗CD3抗体和单核细胞已被证明可导致CD8+ T细胞的扩增效果相似,但诱导的终末分化表型较少,抗原诱导的细胞死亡较少,并且在先前激活的CD8+ T细胞中扩增更多。在制造过程中获得终端分化效应功能实际上可能导致体内抗肿瘤免疫受损。由于T细胞活化和分化的敏感性及其对抗肿瘤免疫和基因工程T细胞寿命的影响,新的方法不断被研究。Expamer技术是一种有趣的新方法,通过使用可溶性的Strep-Tactin多聚体来控制起始和终止时间,该多聚体可以与TwinStrep标签结合的抗CD3和抗CD28 Fab片段组装,并通过添加无毒的D -生物素来解离。可溶添加和灭活的Expamer成分的T细胞活化是特别有吸引力的大规模生产,可能有助于避免过度刺激和随后的细胞凋亡。另一方面,较少刚性的表面用于固定抗CD3/CD28结合物可能是一个更好的选择,因为它们已被证明可以诱导更高的IL-2产生和体外CD4+和CD8+ T细胞的扩增。与此一致,一种抗原呈递细胞(APC)模拟支架由介孔二氧化硅微棒支撑的流体脂质双分子层组成,并附着抗CD3/CD28抗体,与抗CD3/CD28顺磁珠相比,其扩展能力提高了2至10倍。然而,当涉及到大规模生产时,脂质双分子层系统可能不如基于微球的激活方法有吸引力,因为它们在处理和去除方面增加了技术复杂性。为了了解它们对临床疗效的影响,未来需要更多的研究来比较不同激活条件对ACT最终T细胞产物的影响。
基因转移方法
病毒载体被用于所有批准的CAR-T细胞疗法和大多数CAR- T和TCR-T细胞疗法的临床试验,因为它们具有稳定基因转移的效率。慢病毒(LV)和大病毒载体是细胞工程的首选载体,因为与其他病毒载体相比,它们可以携带更大的遗传结构,并将目标基因整合到工程T细胞的基因组中。然而,简化大量病毒载体的生产是一个挑战,并且确保没有残留的病毒载体或意外转导的恶性细胞被给予患者需要广泛和昂贵的安全测试。这给扩大生产规模和使这些疗法更经济实惠以满足对ACT日益增长的需求带来了困难。因此,非病毒方法目前正在早期试验中进行研究。基于转座子的基因传递方法,如睡美人(SB)或PiggyBac(PB)转座子,与病毒载体相比,更便宜,可以携带更大的遗传结构,同时仍然整合其靶基因。SB转位已经在早期临床试验中成功用于制造CD19或SLAMF7 CAR-T细胞,没有严重的毒性。此外,SB换位的自动化是可行的,并且对于大规模生产非常有吸引力。虽然PB转位对于CAR-T细胞的制造也是成功的,甚至显示出促进所需的TSCM CAR-T细胞产生的倾向,但最近的一项临床试验观察到10例患者中有2例形成CAR-T细胞淋巴瘤。这是CAR-T细胞衍生的恶性淋巴瘤的第一例,该研究的研究者对接受CAR-T细胞治疗的患者的定期随访提出了警告,特别是当采用新的基因转移方法时。本研究使用PB系统观察到的恶性转化的潜在原因尚未完全了解。插入突变似乎不是原因,因为CAR转基因的整合模式与其他使用PB的研究相当,并且与使用病毒系统的研究一致。然而,观察到转基因启动子对周围区域的转录上调,但这些改变如何参与恶性转化需要进一步研究。该研究的作者并不认为这一发现是PB系统固有的问题,而可能是基于他们使用高压电穿孔和高浓度转座子和转座酶的制造方法。了解潜在的机制将有助于在未来制定更安全的制造方法和更好的安全读数。基因组编辑是一种很有前途的新方法,不仅适用于产生基因工程的自体T细胞,也适用于“现成的”同种异体T细胞,这可能解决自体T细胞疗法固有的制造挑战和过高的成本。特别是聚集规则间隔短回文重复(CRISPR)-Cas9已被用于癌症患者产生和临床应用具有可耐受不良事件的CAR-T细胞。在未来,多因子基因组编辑对基因工程T细胞的ACT具有巨大的潜力,但需要进一步优化和广泛的安全性监测,以评估有害脱靶事件的风险。关于CRISPR-Cas9基因组编辑用于生成工程T细胞的更多信息见综述。
缩短基因工程T细胞制造时间
优化基因工程T细胞制造过程的一个重要途径是缩短制造时间。这将降低成本,并将扩大生产规模,因为工程T细胞的周转速度更快。最重要的是,它可以减少静脉到静脉的时间,从而降低癌症快速进展患者的死亡率。CAR-T细胞治疗的标准方案是将CAR-T细胞培养11至24天,从而获得大量的CAR-T细胞。有趣的是,在急性淋巴细胞白血病(ALL)的人类异种移植模型中,将CD19 CAR-T细胞的培养时间缩短至仅3天,即使剂量降低6倍,其抗肿瘤活性也会增加。这可能是由于在减少培养时间的CAR-T产物中干细胞样T细胞的比例增加。FastT CAR-T次日制造平台已经实现了显著的制造时间,最近在B细胞ALL的临床试验中进行了评估(NCT03825718)。次日生产,激活,左室转导,无扩张,对所有25例患者都是可行的,具有可耐受的安全性和有希望的疗效。此外,与常规制造的CAR-T细胞相比,CD19 FasT CAR-T细胞在体外表现出更少的衰竭和更年轻的细胞表型,但需要在更大规模的临床研究中进行评估。此外,T-Charge平台在一项I期研究中用于制造CD19 CAR-T细胞,具有良好的疗效和安全性(NCT03960840)。制作时间小于2天,培养时间仅为24小时。这种方法还在最终的CAR-T细胞产品中保存了naïve T细胞和TSCM细胞,这可能会增加基因工程T细胞在患者体内的持久性。CAR-T细胞的快速制造甚至被证明在24小时内不需要激活和扩增,并且在小鼠异种移植模型中显示出比传统制造的CAR-T细胞更高的抗白血病活性。这些新方法似乎有很大的潜力来减少静脉到静脉的时间,这将大大有利于患者。然而,由于大多数T细胞扩增发生在患者体内,这可能意味着不良事件在治疗过程中更难以预测。因此,这些新方法必须在临床试验中进行彻底的测试,并进行严格的监测,以确保与标准的长期制造程序相比,其疗效和安全性没有劣效性。改进和标准化基因工程T细胞的制造方案尤其困难,因为每一步都可能对抗肿瘤活性和安全性产生广泛影响,因为批准的CAR-T疗法的深度制造方案尚未公开。这将是未来的一个挑战,但通过更广泛的交流来克服这一障碍,可能会推动这些突破性新疗法的创新和可及性。
体内靶向基因传递
由于体外T细胞制造的高成本,静脉到静脉的时间长,这对于高度进展的癌症来说是一个问题,以及制造失败的风险,靶向体内T细胞编程可能是一个可行的替代方案。携带DNA的纳米颗粒已被证明可以转运到T细胞的细胞核中,然后在靶向T细胞中表达CAR。此外,在体内使用mRNA纳米载体递送抗肿瘤CAR或抗病毒TCRs,与体外制造的对照品相比,在小鼠体内T细胞中显示了短暂的表达和类似的疾病消退。这些载体系统价格低廉,可以大规模生产,用于更广泛的分布,但它们的安全性和长期疾病缓解的有效性在很大程度上仍不清楚。瞬时表达可能会减少某些安全性问题,例如恶性细胞意外编程并使其对治疗产生耐药性或形成CAR-T淋巴瘤。然而,与体外制造的T细胞相比,缺乏长期T记忆形成可能会阻碍治疗的效果,并可能导致更早的复发。因此,与更成熟的方法(如双特异性T细胞接合剂(BiTEs))相比,它们的疗效可能并不优越。病毒方法也被测试用于体内T细胞的长期编程。腺相关病毒(AAV)载体在人源化小鼠中实现了CAR的导入,并导致肿瘤消退。基于AAV的基因疗法LUXTURNA用于治疗RPE65介导的遗传性视网膜营养不良患者,这是首个获得FDA批准的此类药物,这可能会增加AVV载体在体内T细胞编程治疗癌症的临床应用的兴趣。一项使用CD8α链靶向慢病毒载体(Lv)的研究显示了一种靶向CD19 CAR的体内工程策略。虽然这种方法对CD8 T细胞的特异性很好,但NK和NKT细胞也表现出对CD19 CAR的转导,因为它们也表达靶向CD8α链。利用双特异性抗体串联片段结合Sindbis伪慢病毒载体(SINV-LV)上的突变体E2糖蛋白和T细胞上的CD3,也可以将LV靶向CD3+ T细胞,在人B细胞肿瘤异种移植模型中实现CD19 CAR在体内特异性导入T细胞,具有良好的抗肿瘤效果。尽管病毒体内转导在细胞工程和基因治疗方面取得了早期的临床前和临床成功,但与体外制造基因工程T细胞相比,这种策略的安全风险要高得多,它是否能满足高安全性要求还有待观察。
TCR-T细胞基因转移技术的特殊要求
CAR-T细胞疗法的许多制造工艺的进步很可能转移到TCR-T细胞疗法。然而,产生TCR-T细胞的一个具体问题是,将工程化的TCR引入T细胞可能导致工程化的α或β链与内源性链错配。这带来了不可预测的风险,因为错配的TCRs具有未知的反应性,从未经过胸腺选择,并可能导致形成针对自身肽的TCRs,从而产生自身免疫或移植物抗宿主病(GvHD)。尽管早期保留内源性TCR的TCR- T细胞的临床试验没有观察到GvHD,但预防错配安全风险的方法将是有益的。因此,已经开发了许多策略来避免成功程度不一的错配事件,如图3所示。
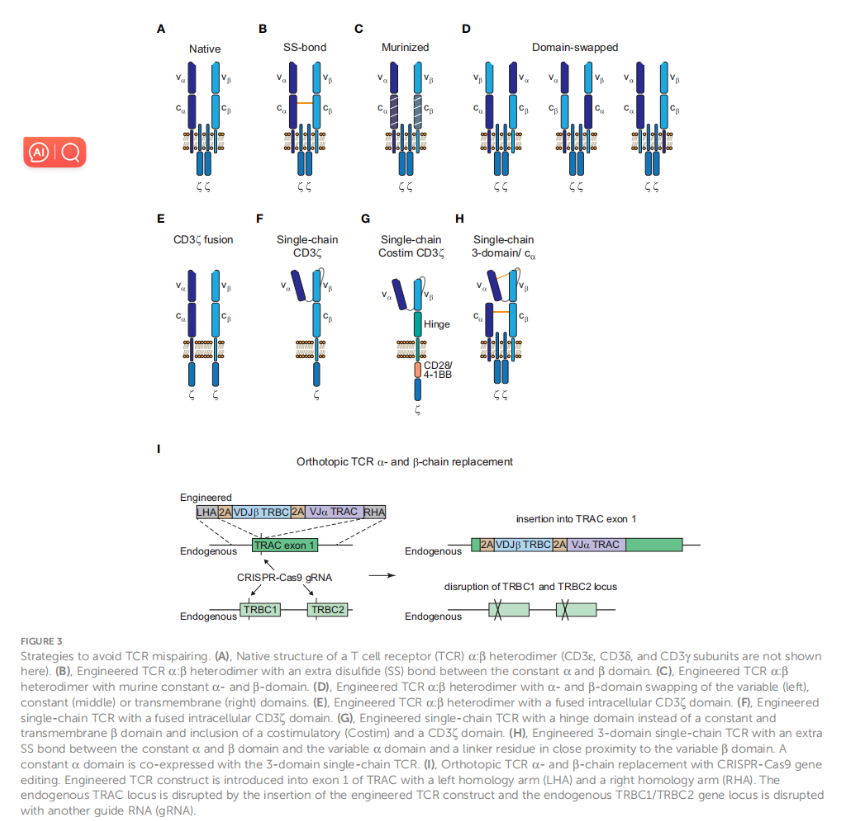
图3 避免TCR错配的策略。(A) T细胞受体(TCR) α:β异源二聚体的天然结构(CD3ε、CD3δ和CD3γ亚基不在图中显示)。(B) 工程TCRα: β异源二聚体,在α和β恒定结构域之间有一个额外的二硫键。(C)具有小鼠α、β恒定结构域的工程TCRα: β异源二聚体。(D) 携带交换α和β结构域可变区(左),恒定区(中)或跨膜区(右)的工程TCR α: β异源二聚体。(E) 具有融合胞内CD3ζ结构域的工程TCR α: β异源二聚体。(F)融合CD3ζ细胞内结构域的单链工程TCR。(G)工程单链TCR,用铰链结构域代替恒定的跨膜β结构域,并包含共刺激结构域(Costim)和CD3ζ结构域。(H),设计的3域单链TCR,在恒定a和β结构域与可变α结构域之间增加了一个SS键,并且在可变区β结构域附近有一个连接子残基。恒定的α结构域与3域单链TCR共表达。(I)利用CRISPR-Cas9基因编辑技术替代原位TCR α链和β链。工程TCR结构通过左同源臂(LHA)和右同源臂(RHA)引入TRAC外显子1。内源性TRAC位点被工程TCR构建体的插入破坏,内源性TRBC1/TRBC2基因位点被另一种引导RNA (gRNA)破坏。在固定结构域中插入额外的二硫键、固定结构域的鼠化化或结构域交换都能减少错配事件,但不能完全阻止错配事件(图3B-D)。只有CD3ζ融合链或单链TCR (scTCR)构建消除错配,但不与内源性CD3γ, δ和ε亚基形成TCR复合物(图3E, F)。据报道,进一步消除恒定β结构域和增加细胞内共刺激CD28或4-1BB结构域类似于CAR的结构和信号传导方式(图3G)。然而,与传统CAR相比,这种结构的改变降低了TCR-CD3复合物的敏感性。因此,最近的scTCR支架试图结合天然CD3复合物的组装,以利用经典TCR信号传导的优势(图3H)。这种3域scTCR由融合到cβ结构域的Vα-linker-Vβ片段组成,并利用cα结构域的共表达,很少发生错配。此外,在Vα结构域和靠近Vβ结构域的连接物残基之间插入二硫键足以防止残余错配。虽然这可能为引入工程TCR提供了一种安全的选择,而没有错配事件的危险,但稳定的scTCR的设计可能会对许多TCR提出技术挑战。稳定性工程可能是解决这一限制的潜在解决方案,因为Vα-和Vβ-结构域的不同区域已经被证明对scTCR的表面表达和稳定性至关重要。如果基因工程T细胞的结构与天然TCR结构有很大的差异,那么改变天然TCR结构可能会导致更高的免疫原性,并降低基因工程T细胞的持久性。因此,在不改变TCR结构的情况下避免错配的另一种方法是敲除内源性的α和β链。原位TCR α链和β链替代(OTR)是通过CRISPR-Cas9基因组编辑完成的,最近在一项I期临床试验中使用新抗原特异性TCR (neoTCRs)在16例难治性实体癌患者中实现内源性TCR替代(图3I)。将工程TCR构建体插入TRAC基因座的外显子1,破坏内源性α链,CRISPR介导的TRBC基因座敲除导致内源性β链破坏。OTR的另一个优点是不与内源性TCR竞争CD3亚基以形成核心TCR-CD3复合物。然而,在某些情况下,使用这种编辑方法,引入的TCR的细胞表面表达可能效率低下。在上述最近的试验中,在为16例患者生成的37个neoTCR中,neoTCR阳性细胞的细胞表面表达率为活细胞产物的1.9 – 46.8%。这可能是方案优化的问题,因为在同一研究中,介质配方和电穿孔装置的改变将敲入效率从13.4%提高到23%。此外,在7号染色体和14号染色体的靶位点观察到染色体畸变,这是潜在的TRAC: TRBC易位的指示。脱靶编辑和靶上突变是CRISPR介导方法的主要关注点,因为它们可能导致编辑细胞的功能改变甚至恶性转化。在临床应用中,密切监测患者将是这些新方法的关键,进一步的努力将是必要的,以了解和减少不必要的DNA畸变 。
基因工程同种异体T细胞
迄今为止,所有被批准的CAR-T细胞疗法都是利用患者来源的自体T细胞。然而,由于只有经过大量预处理的患者才适用于CAR-T细胞免疫治疗,他们的T细胞室经常受损。这可能导致自体CAR-T细胞产物的适应性降低甚至制造失败。此外,针对每位患者的个性化生产具有挑战性,而且成本非常高(如上所述),并且不允许大规模生产以满足对ACT日益增长的需求。“现成的”同种异体T细胞可能是克服这些限制的一种方法。由于未改变的同种异体T细胞可能导致GvHD,同时也会消除患者体内的基因工程T细胞,因此已经开发了许多策略来降低这些风险。对于治疗复发或难治性(r/r) B细胞ALL,异基因CD19 CAR- (NCT02808442和NCT02746952)和CD19/CD22双靶向CAR- T细胞疗法(NCT04154709)已经显示出可控的安全性和抗白血病活性(104,105)。CRISPR-Cas9基因组编辑用于破坏TRAC和CD52基因位点,允许在过继T细胞转移之前使用阿仑单抗进行严重淋巴细胞清除,以降低宿主消除同种异体工程T细胞的风险。在另一项首次人体I期临床试验(NCT04637763)中,异体CD19 CAR-T细胞疗法治疗r/r B细胞非霍奇金淋巴瘤(B- NHL)的早期阳性结果被报道。使用Cas9和CRISPR杂交RNA-DNA (chRDNA)向导进行减少脱靶编辑,引入CD19 CAR到TRAC基因座位,以在此过程中对TRAC基因位点进行破坏。此外,PD-1被敲除,目的是提高基因工程T细胞的持久性和抗肿瘤活性。没有观察到GvHD,治疗通常耐受性良好,临床反应率很好。另一种靶向方法是使用TRAC特异性的ARCUS核酸酶,在特定位点引入破坏构造子,破坏内源性的TCR,以避免GvHD(109)。使用这种编辑方法的同种异体CD19 CAR-T细胞疗法在治疗r/r B-NHL和B细胞ALL的I/IIa期临床试验(NCT03666000)中显示出有希望的结果,并且可能用于治疗先前接受自体CAR-T细胞治疗的淋巴瘤复发患者。所有11例患者在6个月后均显示客观缓解率(ORR),但未报告GvHD。基因组编辑还允许产生抗自杀型的CAR-T细胞。在一项I期临床试验(NCT04538599)中,CD7 CAR – T细胞疗法用于治疗T细胞淋巴瘤和表达CD7的急性髓性白血病(AML)。由于CD7也在正常T细胞上表达,因此CD7被敲除以避免自杀,并进行了一些额外的编辑(敲除TCR和HLA-II,敲入NK细胞抑制剂)以避免同种异体CAR-T细胞产物的GvHD。同种异体TCR-T细胞也在一项研究者发起的I/II期临床试验(NCT01640301)中成功测试,用于接受同种异体造血细胞移植(HCT)的高风险复发AML患者。来自HCT供者的EBV特异性CD8 + T细胞被TCR转导,该TCR可识别AML相关的细胞内抗原Wilms肿瘤抗原1(WT1)。HLA-A*0201表达的患者接受同种异体HCT,在HCT后第28天未检测到疾病,预防性给予工程化WT1特异性T细胞。所有12例患者的中位无复发生存期为44个月,与88例患者的54%无复发生存期相比非常有利。这些结果鼓励使用同种异体巩固ACT作为预防HCT后AML复发的策略。此外,同种异体HA -1特异性TCR – T细胞在接受同种异体HCT治疗的r/r ALL患者中,对HLA-A*0201阳性患者的治疗效果,目前正在一项剂量递增研究中进行探索(NCT03326921)。关于它们的疗效和GvHD的风险,我们在这里描述的同种异体工程T细胞的早期临床研究的初步结果令人鼓舞,但是这种方法仍处于早期阶段,我们需要等待更大的临床研究来评估其临床价值。
改善CAR-T和TCR T细胞治疗的当前挑战和潜在策略
CAR-T细胞疗法在某些B细胞恶性肿瘤中表现出显著的疗效,但在髓系恶性肿瘤和实体肿瘤中却表现不佳。CAR-T和TCR-T细胞疗法面临的挑战限制了它们的临床疗效,包括严重的不良事件、有限的肿瘤浸润、基因工程T细胞的持续存在,以及抗原丢失导致的肿瘤免疫逃避。特别是,实体肿瘤中免疫抑制性TME的复杂性限制了T细胞的浸润,并通过在肿瘤细胞上呈现抑制性配体来促进T细胞的衰竭。有许多方法旨在通过克服肿瘤抗原逃逸和增加肿瘤特异性来改善ACT,这里将重点介绍一些策略的选择(图4)。
与基因工程T细胞相关的不良事件
基因工程T细胞免疫疗法通常伴随着中度到严重的不良事件,限制了它们在某些病例中的临床应用。工程化T细胞治疗最常见和最严重的不良事件是细胞因子释放综合征(CRS),这是在临床研究中首次观察到的,当时未在临床前模型中发生。此外,免疫效应细胞相关神经毒性综合征(ICANS),通常被称为神经毒性,在接受CD19 CAR-T细胞治疗的患者中非常常见。CRS的症状范围从轻度发烧到危及生命的表现直至多器官系统衰竭。对接受工程化T细胞治疗的患者进行随访并监测CRS体征,对于单独使用抗IL – 6受体激动剂tocilizumab或联合皮质类固醇治疗中重度CRS病例至关重要,并给予广泛的支持治疗。ICANS的症状包括头痛、脑病、震颤和癫痫发作,这些症状通常是自限性的,但也有罕见的致死病例报道。严重病例通常使用皮质类固醇治疗,而托珠单抗对ICANS的治疗大多无效,与其在CRS中的有效性相反。工程化T细胞与其他免疫细胞,特别是巨噬细胞之间的相互作用可导致CRS形式的全身性炎症的诱导,这可能导致血脑屏障渗漏和ICANS症状。因此,ICANS通常与患者CRS的严重程度相关,但也有报道称在一些没有CRS的病例中也存在ICANS。靶向非肿瘤毒性是过继性T细胞疗法的另一个挑战。与CRS和ICANS相比,这种不良事件不是由相关的内源性免疫细胞间接引起的,而是由工程T细胞识别其同源抗原或健康组织上的交叉反应性抗原直接引起的。特别是,在针对MAGE-A3阳性癌症的两项早期临床试验中,TCR-T细胞需要仔细筛选,以避免由于心脏和大脑组织损伤致死病例而引起的自身反应性严重毒性。由于这些TCR的亲和力增强,靶外肿瘤毒性可能增加。然而,最近针对MAGE-A4的亲和性增强TCR的研究显示,在没有严重TCR- t细胞介导的毒性的情况下,临床疗效良好,这表明有必要研究每种单一修饰的TCR是否存在此类风险,尽管未修饰的TCR也有交叉反应性的潜力。这些病例突出了TCR候选药物筛选方法的困难,以排除潜在的常见和个体化严重自身反应性,这在临床前水平很难得到充分的测试,但也表明TCR有可能代表具有良好疗效的安全疗法。对于使用同种异体CAR-T和TCR-T细胞,潜在的额外不良事件风险是同种异体工程T细胞对外来MHC分子或宿主细胞上的次要组织相容性抗原的同种异体反应性,可导致GvHD。如上所述,早期临床试验表明,基因编辑去除内源性TCR是避免GvHD的可行策略。此外,在HCT后使用同种异体工程T细胞,供体细胞HLA的配型,以及使用非αβ T细胞是潜在的策略。然而,由于宿主免疫系统对同种异体T细胞的消除是一个严重的问题,因此与这些策略相比,同种异体工程T细胞的持久性有多强还有待观察。此外,伴随治疗,如T细胞治疗前的淋巴细胞清除,会增加血液学毒性,如细胞减少症,这是一种常见的不良事件,通常原因不明。总的来说,这突出了CAR-T和TCR-T细胞治疗的不良事件的复杂临床前景,以及需要更好的临床前模型来早期预测它们。
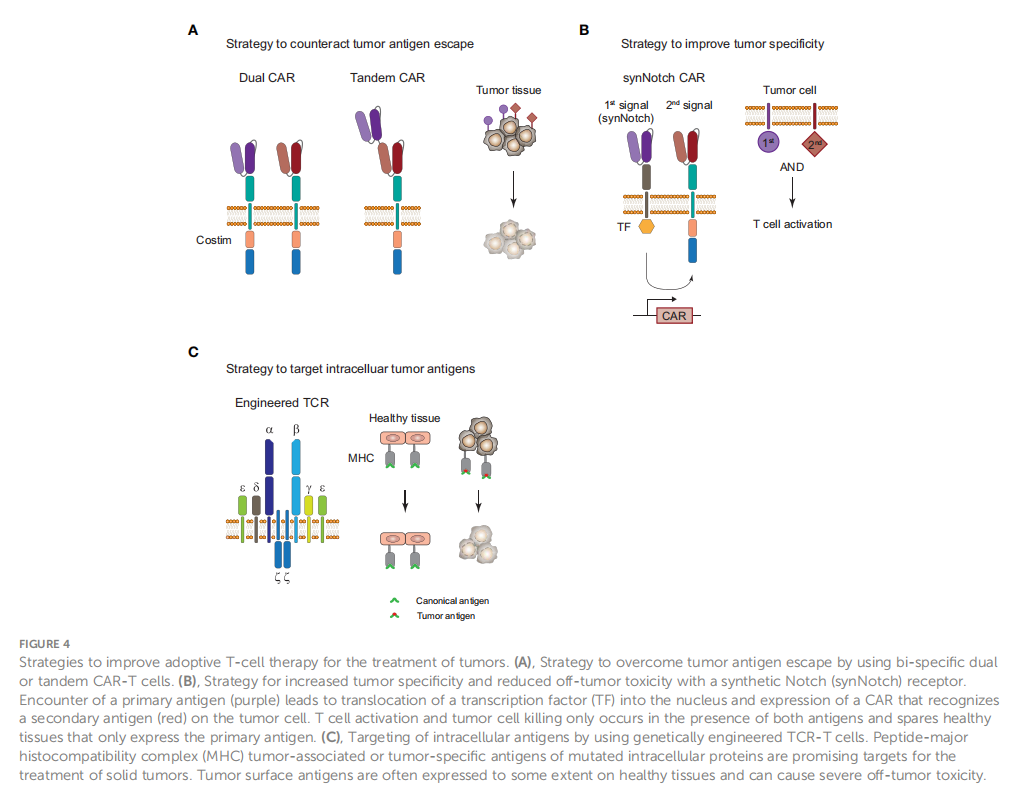
图4 改进过继T细胞治疗肿瘤的策略。(A) 利用双特异性双或串联CAR-T细胞克服肿瘤抗原逃逸的策略。(B)合成Notch (synNotch)受体提高肿瘤特异性和降低肿瘤外毒性的策略。初级抗原(紫色)的相遇导致转录因子(TF)易位进入细胞核,并在肿瘤细胞上表达识别次级抗原(红色)的CAR。T细胞的活化和肿瘤细胞的杀伤仅在两种抗原存在的情况下发生,而只表达初级抗原的健康组织则不受影响。(C) 利用基因工程TCR-T细胞靶向细胞内抗原。多肽-主要组织相容性复合体(MHC)肿瘤相关或肿瘤特异性突变的细胞内蛋白抗原是治疗实体瘤的有希望的靶点。肿瘤表面抗原通常在健康组织上有一定程度的表达,可引起严重的肿瘤外毒性。
基因工程T细胞的持久性
据报道,两名慢性淋巴细胞白血病患者在缓解后CD19 CAR-T细胞持续存在长达10年。虽然CD8+ CAR-T细胞在最初的反应中被大量发现,但在长期缓解期间,几乎只有CD4+ CAR-T细胞存在。然而,在许多针对多种肿瘤实体的CAR-T和TCR-T细胞临床试验中,已经报道了T细胞持久性差,这通常可能是临床疗效有限或复发的原因。因此,通常在工程化T细胞治疗之前进行淋巴消耗方案,以增加T细胞的持久性。临床前研究发现,PD-1敲除后,CAR-T细胞耗竭减少,抗肿瘤活性提高。因此,目前正在探索将PD-1敲除用于CAR-T和TCR-T细胞治疗肿瘤,作为保护工程T细胞免于衰竭并增强其持久性的策略。Stadtmauer等人利用CRISPR-Cas9基因组编辑去除内源性TCR和PD-1,并引入一种针对癌睾丸抗原(CTA)NY-ESO-1和LAGE-1的工程化TCR,治疗了2例难治性黑色素瘤和1例肉瘤。在两名黑色素瘤患者身上观察到,工程T细胞被运送到肿瘤部位,靶抗原减少,可能是对TCR-T细胞免疫压力的反应。有趣的是,与之前的T细胞保留内源性TCR和PD-1表达的试验相比,在所有3例患者中,至少9个月没有观察到毒性,TCR-T细胞的持久性都增加了。然而,这项第一非人类I期临床试验的患者数量很低(NCT03399448),扩大研究是必要的。这种持续时间的延长是基于PD-1的消融还是部分基于内源性TCR的去除,还有待阐明。此外,PD-1消融也被报道在CD19 CAR-T细胞治疗中,随着更大的活化,导致功能衰竭和细胞死亡增加。慢性淋巴细胞性脉络丛脑膜炎病毒(LCMV)感染小鼠的PD-1敲除实验结果表明,CD8+ T细胞耗竭不仅可以在PD-1缺失的情况下发生,而且PD-1甚至可以保护细胞免受过度刺激和终末分化,在感染部位产生耗竭效应表型。这表明PD-1可能与特定环境中微调T细胞反应有关,例如病毒感染中的高抗原负荷。在这种情况下,ICI对PD-1的短暂阻断可能优于PD-1消融,但我们对PD-1信号在T细胞反应中如何调节基因表达的理解仍然是谜,需要进一步阐明。最近的一项研究表明,与生存和增殖相关的基因对PD-1介导的抑制具有抗性,而基于TCR信号强度的效应功能则受PD-1调控。由于PD-1信号的上下文依赖功能,PD-1消融基因工程T细胞是否是根据肿瘤实体和抗原负荷改善T细胞持久性的有效方法还有待观察。此外,据报道,一些共刺激开关受体可以防止基因工程T细胞的衰竭,并可能增加它们的持久性。开关受体由抑制受体的细胞外部分(如PD-1、TIGIT、TIM-3)和共刺激受体的细胞内信号域(如CD28,4–1BB)组成。来自临床前研究的报告令人鼓舞,具有这些开关受体的基因工程T细胞的抗肿瘤活性和持久性得到了改善,然而,这些信号轴在本质上是复杂的。像抗PD-1/PD-L1 ICI那样,从衰竭到激活的天平倾斜,不仅仅是平衡,可能导致过度刺激和功能失调的T细胞表型。在最近的研究中,补源性TCR信号也与CAR-T细胞的持久性改善有关。在一项涉及15名患者的I期临床试验中,去除间皮素(MPTK)特异性CAR-T细胞中的内源性TCR和PD-1用于治疗实体肿瘤,导致6周以上TCR缺陷的CAR-T细胞的持久性较差 (NCT03545815)。令人惊讶的是,TCR阳性的CAR-T细胞在三名患者的输注后成为主要部分,尽管它们在输注的细胞产物中很少出现。作者在小鼠中重复了这些发现,并假设补益TCR信号在CAR-T细胞的持久性中起着有益的作用。值得注意的是,这是在低水平植入的情况下,当使用淋巴清除来增加植入时可能会有所不同。与这些观察结果一致,另一项研究也观察到动物模型中TCR缺陷CD19 CAR-T细胞的持久性降低。补性TCR信号在CAR-T细胞寿命中的作用需要进一步研究,特别是在同种异体CAR-T细胞治疗的背景下,去除内源性TCR已经是预防GvHD的常见做法。Statdmauer等人的结果表明,内源性TCR替代的TCR- T细胞可能不受引入TCR的滋补信号的影响。
克服肿瘤抗原逃逸的潜在策略
肿瘤对ACT耐药的一种常见形式是肿瘤抗原通过表面抗原或肽-HLA复合物的丢失或下调而逃逸。通过双CAR或串联CAR的工程T细胞靶向多种抗原可以降低肿瘤抗原逃逸的风险(图4A)。CD19/CD22双特异性CAR的I期研究(NCT03233854)的初步结果显示临床疗效,但复发时抗原逃逸主要是针对CD19而不是CD22抗原,这表明CAR- T细胞对CD22靶点的免疫压力较小。CD22 scFV在双特异性CAR中的连接显示比CD19 scFV更少的细胞因子分泌,这一观察结果支持了这一点。另一种使用串联方法的双特异性CD19/CD22 CAR在6例r/r B-ALL患者中显示出良好的疗效,并在治疗5个月后观察到一次原始细胞复发,CD19抗原丢失和CD22表达减少(NCT03185494)。多特异性CAR- T细胞的单结构方法可能会影响基于连接体设计的抗原结合能力,因此使用双或三顺反子设计在同一细胞上表达单个CAR分子可能是有利的,以避免这些问题。这已经在体外和动物模型中用于三联体CD19/CD20/ CD22三特异性CAR-T细胞,这些细胞能够独立于CD19表达靶向B系ALL。一项使用双链CD19/CD22双特异性CAR-T细胞治疗15例r/r B-ALL患者的I期研究(NCT03289455)的结果显示,CR为86%,一年总生存率和无事件生存率分别为60%和32%(139)。在肺癌和黑色素瘤异种移植模型中,双靶向多种实体肿瘤中过表达的B7-H3和CD70,用串联CAR诱导了优越的肿瘤控制和总生存率。此外,向患者输注不同特异性的单特异性CAR-T细胞或TCR-T细胞的混合物也可能是一种可行的选择,最近已经在实体肿瘤患者中进行了试验,该患者接受了多达三种不同特异性的新TCR-T细胞。不同抗原的多重靶向似乎是克服肿瘤抗原逃逸的可行策略,初步结果表明它可能增加对共表达多种抗原的肿瘤细胞的抗肿瘤免疫。然而,这种方法目前受到已知有希望的肿瘤抗原数量的限制,未来将受益于发现更多的肿瘤相关抗原和肿瘤特异性抗原。
实体瘤治疗的潜在策略
实体瘤的治疗是该领域最困难的领域之一。有限的T细胞浸润到肿瘤中,以及由于免疫抑制TME引起的T细胞衰竭,使得对治疗反应不足的风险很高。此外,实体瘤中抗原表达的异质性和缺乏真正的肿瘤特异性表面抗原可在健康组织中引起严重的肿瘤外毒性。由于很难识别实体肿瘤上的肿瘤特异性表面抗原作为CART细胞治疗的靶点,因此已经开发出了具有更高特异性和更低肿瘤外毒性的策略,例如合成Notch(synNotch)受体设计(图4B)。synNotch受体对初级抗原的识别会从细胞质尾部切割出一个正交转录因子,并诱导肿瘤细胞上能够识别次级抗原的CAR的表达。只有当两种抗原都在肿瘤细胞上表达时,T细胞激活和肿瘤细胞杀伤才会发生。这一概念已应用于许多实体瘤模型的临床前研究,并证明了实体瘤治疗的特异性提高。SynNotch电路还可用于提高工程TCR选择性杀死肿瘤细胞的特异性,这已被证明用于体外对抗黑色素瘤细胞的SynNotch-TCR。TCR-T细胞天生具备通过肽- HLA呈递识别细胞内抗原的能力,这为TCR-T细胞治疗实体瘤开辟了肿瘤相关或肿瘤特异性抗原的宝库(图4C)。如前所述,一项初步研究表明TCR-T细胞在2例黑色素瘤和1例肉瘤患者(70例)中的可行性和有效性,而在MAGE-A4阳性实体瘤的临床试验中,TCR-T细胞在部分患者的临床疗效中ORR为24%。Foy等人最近证明了靶向个体化新抗原的TCR-T细胞治疗的可行性。采用全外显子组测序(WES)和患者肿瘤RNA测序的组合筛选方法预测潜在的新抗原。下一步,多聚体标记肽-HLA复合物被生成,用于评估患者外周血中预测的新抗原的反应性,并为16名患者鉴定和制造了新抗原。尽管这种复杂的工作流程在临床环境中的可行性令人印象深刻,但疗效和T细胞持久性是有限的。然而,在clinicaltrials.gov上注册的过继性TCR-T细胞转移的临床试验超过100项,其中大多数用于治疗实体瘤。TCR-T细胞治疗的障碍包括它依赖于特定的HLA基因型,在大多数情况下限制它只适用于特定的患者群体,以及它对HLA下调的易感性。此外,细胞内抗原也可以用TCR样CAR靶向,这些CAR使用识别特定肽- MHC复合物的scFV分子。最近,一项针对MAGE-A4肽-HLA-A*02:01复合物的TCR样CAR-T细胞疗法治疗实体瘤的I期临床试验已经启动,在临床试验中评估更多TCR样CAR格式的临床疗效将对这一概念的使用产生极大的兴趣。总的来说,为了克服其复杂的免疫逃避机制,未来治疗实体瘤可能需要采用多种不同干预措施的组合方法。
未来展望
利用基因工程T细胞的过继免疫疗法治疗难治性肿瘤是一种新的突破性治疗方法,在某些癌症中具有良好的疗效。然而,它的应用受到制造困难、严重不良事件、监管挑战和极高成本的阻碍。目前有许多策略可以解决这些限制。自动化和加速的制造过程可能对产品质量和成本都有影响。使用同种异体供体T细胞的方法可以提高可用性,但也提供了“现成”的治疗方法,因此大大降低了成本。由于TCR-T细胞疗法的HLA限制,公司似乎不太可能经历昂贵的过程,在CAR-T细胞疗法目前已经显示出良好疗效的肿瘤类型中测试这种疗法。因此,TCR-T细胞主要在实体肿瘤中进行测试,而实体肿瘤缺乏良好的表面靶点限制了CAR-T细胞治疗。目前,TCR-T细胞通常靶向肿瘤相关抗原,但首次肿瘤特异性研究已经证明了它们的可行性,个性化方法可能在未来更为普遍。由于与CAR-T细胞相比,TCR-T细胞具有更高的抗原敏感性,特别是对于亲和性增强的TCR细胞,因此改进预测潜在靶外肿瘤毒性的工具对TCR-T细胞尤其重要。这对于节省临床翻译新鉴定、优化或个性化TCR结构的时间尤为重要。此外,开发新的临床前模型来预测相关不良事件,如CRS和ICANS,对于开发新的策略来排除未来临床试验前最严重的不良事件是必要的。探索新策略的临床研究的数量和该领域创新的速度令人印象深刻。然而,对这些新型和复杂疗法的监管很难跟上这种速度,某些制造步骤的标准化可能是必要的,以确保未来患者使用T细胞产品的安全性和可比性。为了使这些疗法更普遍地可用,并探索它们不仅对难治性肿瘤而且对疾病早期阶段的益处,它们的制造成本和资源必须为卫生保健系统变得更可持续。其中一个主要的挑战是在抗药性的情况下开发新的策略。针对多种抗原和中和免疫抑制TME的个性化组合方法可能是治疗实体瘤和未来耐药血液系统恶性肿瘤所必需的。结合基因工程T细胞的ACT主要用于治疗癌症,但其治疗其他疾病的潜力也越来越被人们认识到。CD19 CAR-T细胞治疗难治性系统性红斑狼疮(SLE)患者的初步结果显示其耐受性良好且高效。探索其在其他自身免疫性疾病和遗传疾病中的应用,可能会为未来治疗失败开辟有效的新选择。