《细胞》:一箭双雕!一针癌症疫苗让CAR-T疗法突破壁垒,有望“完全清除”实体肿瘤
来源:细胞、学术经纬 | 发布时间:2023-07-06
通过改造自身来源的T细胞,让其能够更精准地靶向癌细胞发挥作用,这是嵌合抗原受体T细胞(CAR-T)疗法最具突破性的抗癌策略。全球范围内,已有多款CAR-T疗法获批,在面对以往束手无策的恶性肿瘤,尤其是血液肿瘤时,医生有了新的武器。
当然,现有的CAR-T疗法仍然具有改进和拓展的潜力:一方面是增强CAR-T细胞进入体内后的功能,比如延长其抗癌持续时间;另一方面便是向着攻克实体瘤的目标前进,使得CAR-T疗法在更多肿瘤类型中发挥作用。
经过改造后,CAR-T细胞会靶向一个特定的肿瘤抗原,这个肿瘤抗原就像指路的明灯。但随着癌细胞的演化,有些癌细胞会选择不再表达这一抗原,这意味着它们会从CAR-T细胞手下逃脱。
图片来源:123RF
麻省理工学院Darrell Irvine教授和马乐园博士团队在数年前就开始尝试解决这一问题,他们于2019年提出了一种疫苗策略,即通过额外的一针增强剂来刺激CAR-T细胞。其原理是让肿瘤抗原与脂质载体结合,注射后随身体循环系统运输到淋巴结处。在这里,CAR-T细胞会被相匹配的抗原激活。
在当年发表于《科学》的论文上,研究团队展示了这一策略的有效性,在CAR-T细胞输注后的第二天和一周后给予疫苗注射,可以使CAR-T细胞种群在两周后继续扩增,并且清除小鼠体内的胶质母细胞瘤。

时隔3年,研究团队再次在《细胞》杂志发文,揭示了疫苗发挥作用的背后机制。在描述结果时,作者提到了一个“抗原扩散”(antigen spreading)的概念,即疫苗不仅激活了CAR-T功能,更使得宿主的其他T细胞同时得到激活,并且这些T细胞可以靶向其他的肿瘤抗原,解决了此前CAR-T清除不够彻底的问题。

在最新研究中,实验小鼠在CAR-T输注24小时和一周后接受了疫苗接种。根据作者的观察,疫苗的加入可以显著提升小鼠内源抗肿瘤CD4+和CD8+T细胞的数量和功能。
除此之外,CAR-T细胞在接受疫苗刺激之后本身也会发生一些变化,其中起到关键作用的是,干扰素-γ的生产水平会得到极大的提升。高水平的干扰素赋予了CAR-T细胞很强的耐受性,尤其是在面对免疫抑制的肿瘤微环境时,CAR-T细胞能更好地发挥作用。
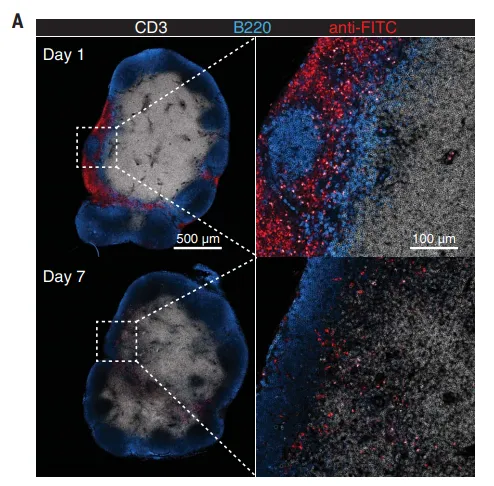
▲疫苗成分会在淋巴结集结,并刺激CAR-T细胞
除了CAR-T细胞,小鼠自身的免疫细胞(尤其是内源T细胞)也会被激活。像实验中的CAR-T细胞专门识别肿瘤细胞表面EGFRvIII蛋白,而其他内源抗肿瘤T细胞可以识别另外的肿瘤抗原,双方共同作用可以极大地提升肿瘤清除效率。
作者发现,如果没有疫苗激活并扩增自身抗肿瘤T细胞,那么即使CAR-T治疗可以清除大部分癌细胞,肿瘤仍然会复发生长。在测试中,即使小鼠携带的肿瘤中只有80%的细胞携带了CAR-T靶向的EGFRvIII抗原,但在疫苗的刺激下通过遗传学手段进一步加强CAR-T干扰素-γ的生产水平,最终80%的小鼠个体实现了肿瘤完全清除。
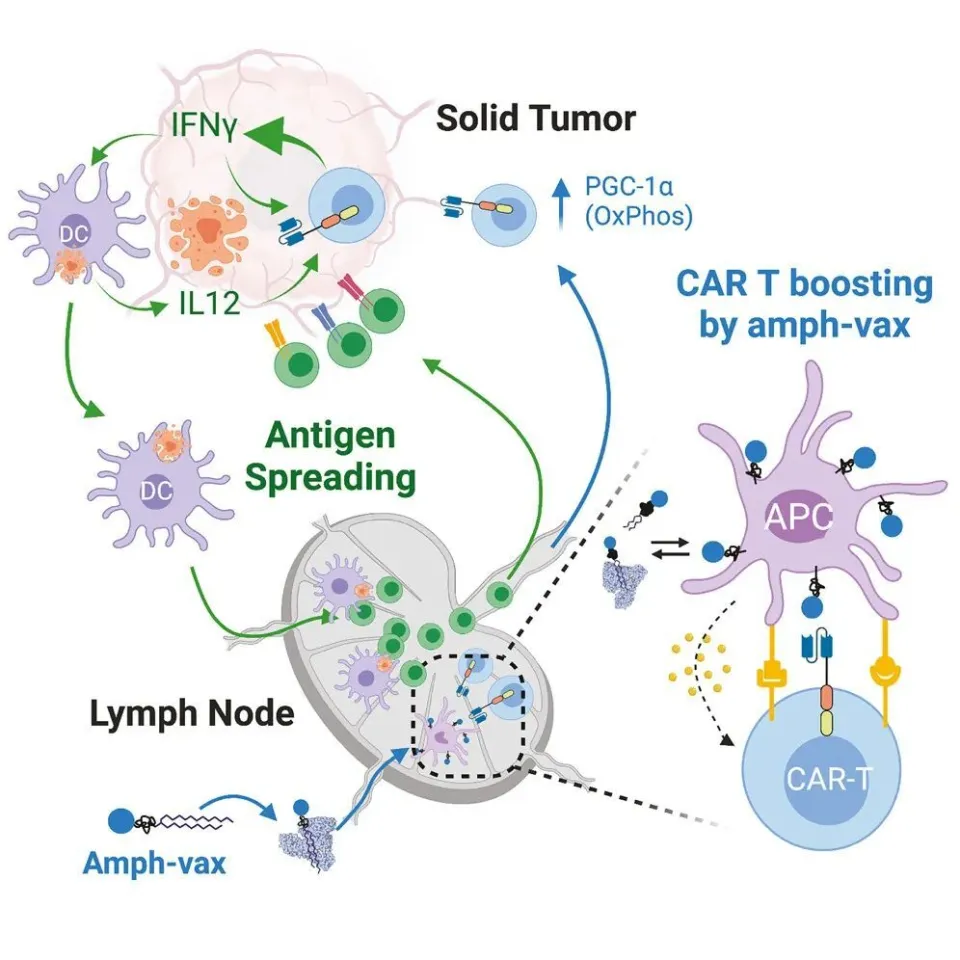
▲研究示意图
研究指出,一些实体瘤中表达特定的抗原靶点的癌细胞比例可能高达90%,这意味着疫苗加CAR-T的联合疗法有望突破实体瘤壁垒,给更多癌症患者带去治愈希望。