新冠口服药热门靶点“江湖对决”,谁更胜一筹
来源:药智头条 | 发布时间:2023-01-31
近日,有两则新冠相关新闻值得关注:第一则是关于两把斩杀病毒的利剑获批上市:1月29日,国家药监局按照药品特别审批程序,附条件批准海南先声药业有限公司申报的1类创新药先诺特韦片/利托那韦片组合包装(商品名称:先诺欣)、上海旺实生物医药科技有限公司申报的1类创新药氢溴酸氘瑞米德韦片(商品名称:民得维)上市。
图1. 国家药监局附条件批准新冠病毒感染治疗药物先诺特韦片/利托那韦片组合包装、氢溴酸氘瑞米德韦片上市
第二则是预防新一轮疫情的盾牌:1月26日,美国FDA一个由21名专业委员组成的疫苗与相关生物制品咨询委员会(VRBPAC),发起了一项匿名投票,最终以21:0通过了支持将现行的”基础针+加强针”的新冠疫苗注射流程,优化为每年只需接种一剂二价新冠疫苗(原始毒株加奥密克戎BA.4/BA.5毒株)。
2款进口新冠药物谁是赢家
从全球市场上看,再生元和礼来的针对原始毒株的抗体药物对目前流行的新毒株无效,而有潜在致突变风险的默沙东的莫诺拉韦口服抗病毒药物治疗新冠肺炎的临床表现并不算太理想。
去年上半年,辉瑞新冠口服药物在美国市场销售额反超默沙东卖出了96亿美元。分析人士预计辉瑞的新冠肺炎疫苗和口服抗病毒药物的总峰值销售额可能会在500亿至600亿美元之间。
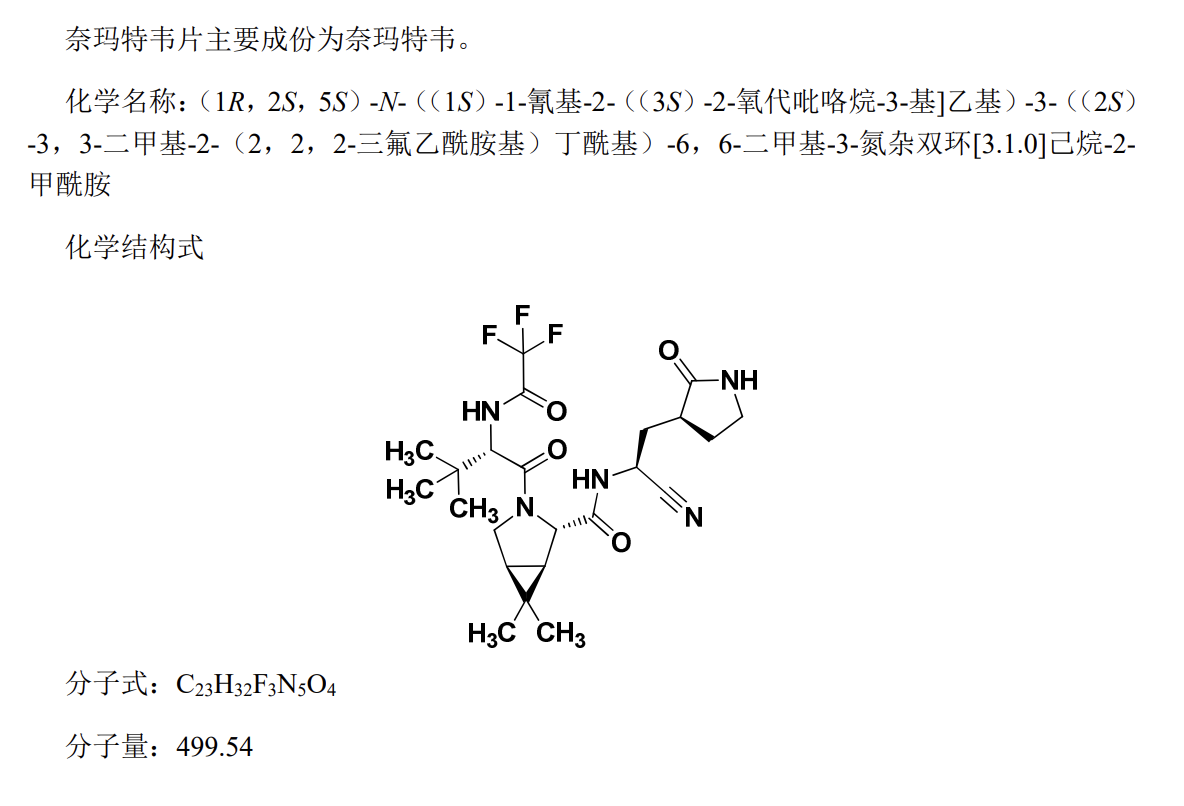
图2. 辉瑞P药阻断病毒复制的奈玛特韦化学结构。
早在2021年4月,辉瑞就公布了后来成为P药主要成分的奈玛特韦(PF-07321332)的结构。此药物是原先用于开发用于治疗冠状病毒FIPV导致的猫腹膜炎的模拟多肽类似物。
根据资料显示奈玛特韦是通过修改前期临床候选药物PF-07304814而开发的。它是一种可逆的共价抑制剂,可与一种主要蛋白酶的半胱氨酸残基发生反应PF-07304814需要静脉注射必须在医院使用。但奈玛特韦通过一系列碳链成环,添加氟改善吸收,最终优化为可以口服的药物。进一步研发发现奈玛特韦容易被肝脏分解,于是采用复方,与减缓肝脏的细胞色素酶对奈玛特韦的代谢的利托那韦同时使用,以维持奈玛特韦的起效浓度。
但国家医保药品目录谈判中,辉瑞奈玛特韦片/利托那韦片组合包装因报价高未能成功。不过最近辉瑞首席执行官艾伯乐表示,该公司将继续与国内伙伴合作,推动在中国生产这一款新冠药物。
3款国产新药各自有何特点
阿兹夫定
由河南真实生物科技有限公司和上海复星医药股份有限公司共同研发销售的阿兹夫定片,最早是由河南师范大学的常俊标教授领衔研发的一款抗HIV药物。此药物属核苷类小分子药物,有逆转录酶抑制剂、RNA病毒聚合酶活性抑制剂。
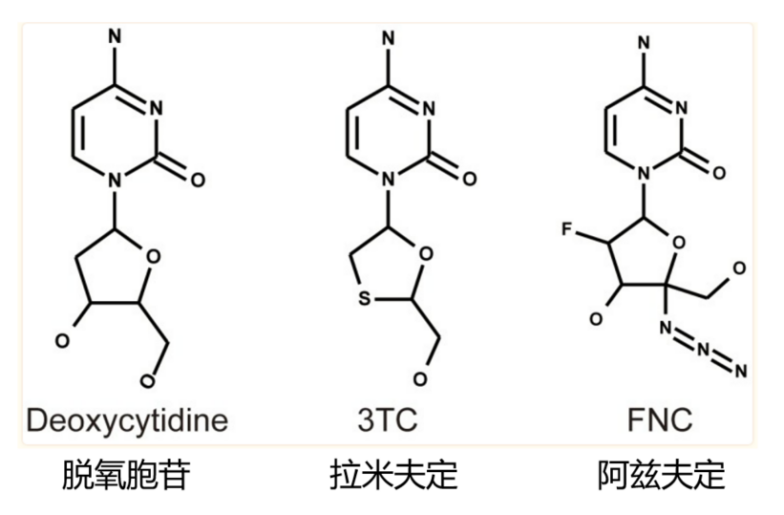
图3. DNA成分之一脱氧胞苷,治疗艾滋病药物拉米夫定和阿兹夫定的结构。
去年7月25日,药监局应急附条件批准阿兹夫定片用于治疗普通型冠病成年患者;8月9日,阿兹夫定被正式纳入第九版冠病诊疗方案。
随着去年年底疫情管控大幅放宽,相应药品出现短缺,尤其是辉瑞生产的Paxlovid不仅价格昂贵,还非常稀缺的情况下,阿兹夫定成为了可解燃眉之急的选择。
但值得关注的是这类核苷类逆转录酶抑制剂往往与我们体内的脱氧核糖核苷酸结构非常类似,它与逆转录酶结合后可以阻断病毒复制。在药企研发的Y博指出这类药物必须重点关注遗传毒性与生殖毒性问题。
事实上,CDE去年6月30日公示了阿兹夫定片的申请上市技术审评报告和说明书,明确提到了阿兹夫定具有遗传毒性和生殖毒性。值得一提的是默沙东的莫诺拉韦(Molnupiravir)也有遗传毒性和生殖毒性的担忧。
不过笔者认为在无药可用特殊时期,作为一个新冠治疗药物,阿兹夫定的用药周期相对较短,按照推荐用药周期不超过一周,对于未怀孕的成人和有重症风险的老人能起到早期阻断病毒复制的效果,有一定效果但也要注意风险。
今年1月8日,在国家医保药品目录谈判工作结束后,国家医疗保障局医药管理司负责人介绍阿兹夫定片谈判成功参与医保药品目录。
先诺欣(SIM0417)
先诺欣(先诺特韦片/利托那韦片组合包装)是由先声药业和上海药物研究所、武汉病毒研究所联合开发的抗新冠病毒创新药。根据官网披露的研究结果,此药对中国轻至中度新冠成年患者安全有效,有显著的临床疗效主要包括以下三点:
- 加快症状恢复,缩短病程
- 显著的抗病毒效果
- 核酸转阴时间缩短
详细数据预计未来在学术期刊或会议上予以公布。
和辉瑞的P药类似,先诺欣也是一个复方制剂,由3CL蛋白酶抑制剂先诺特韦片和抑制肝脏的CYP代谢酶的药效增强剂利托那韦组成。其中,先诺特韦片是对抗新冠病毒的主力选手,其通过抑制剂3CL蛋白酶的活性,导致病毒蛋白前体不能裂解和形成成熟病毒体,终止自我复制过程,从而达到阻止病情进展的目的。
不过有业内人士指出,在临床试验中先诺新的给药剂量是辉瑞药物两倍多,考虑到辉瑞药物的起效成份是共价抑制剂,而先诺特韦基于辉瑞早起多肽结构设计的非共价抑制剂可能存在活性不够好和代谢不稳定的劣势,而又同时模仿辉瑞联用利托那韦,也会造成上文列出的多款药物相互作用导致使用受限的问题。
民得维(VV116)
抗新冠药氢溴酸氘瑞米德韦片(VV116)是针对新冠病毒高度保守的RNA依赖性RNA聚合酶(RdRp)设计的广谱病毒复制阻断剂。灵感来源于瑞德西韦,当年是由杨台莹博士团队开发,除了100mg活性成分瑞德西韦外,还有环糊精钠作为增溶剂。同样是出自上海药物所的沈敬山科研团队在去年8月发表了VV116的合成论文,介绍了通过设计合成GS-441524类似物的一系列具有广谱抑制新冠病毒的化合物,其中就包括巧妙规避了吉利德专利的氘化核苷药物VV116。
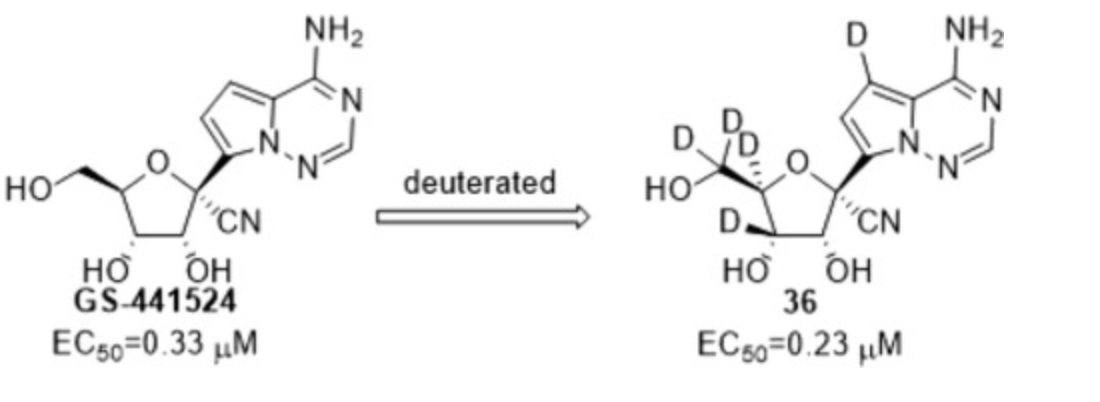
图4. 药化论文中给出的氘化衍生物结构和活性。
(VV116是一个氘代药,即一些氢原子改成了同位素氘。这种改进一方面可以改善药物代谢特征,让一些药物在体内维持时间更久,另一方面也可以规避专利。)
当然医药同行关于民得维的临床设计也有一些争议,包括对照药临床终点。
但从药物机理上来说口服此药在体内转化为GS-441524这一研究透彻的活性成分,是目前学术界公认相对安全有效的广谱冠状病毒阻断剂。而且相比需要注射给药的瑞德西韦,口服药物VV116具有更方便下放到社区使用,避免医疗挤兑的发生。基于当初为了抗击埃博拉病毒而开发失败的GS-441524如今成为拯救猫咪腹膜炎和新冠病毒的有效药物也算是一大幸事。
关于三者的结构和资料总结如下。
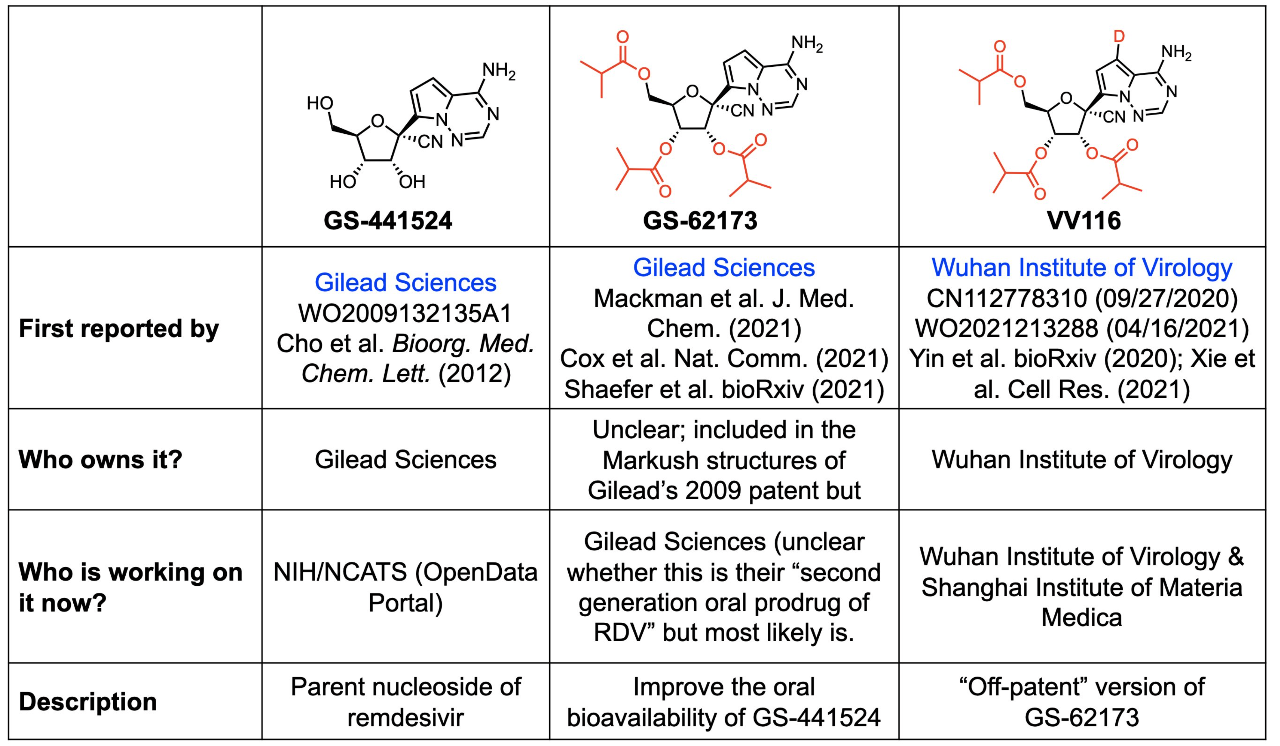
图5. 瑞德西韦活性成分GS-441524与专利结构GS-62173和VV116的对比
4款临床三期新冠药物进展
目前还有4款国产口服小分子新冠药物处在三期临床阶段,分别为众生药业RAY1216,前沿生物FB2001,广生堂GST-HG171和开拓药业普克鲁胺。
众生药业RAY1216
一项研究者发起、RAY1216治疗新冠感染患者的剂量探索性研究中,提示RAY1216片单药组或联合利托那韦组均较安慰剂组可快速降低新冠病毒RNA载量和缩短病毒核酸转阴时间(二者均有统计学显著性差异)。
就RAY1216片Ⅲ期临床研究进展,众生药业1月2日公告,公司控股子公司广东众生睿创生物科技有限公司组织开展的一类创新药物RAY1216片,其用于轻型和普通型新冠病毒感染患者的随机、双盲、安慰剂对照III期临床研究,已经按临床方案要求,完成全部病例数入组。
前沿生物FB2001
1月2日,前沿生物公告,目前公司正在积极加速推进注射用FB2001拟治疗新冠病毒感染住院患者的II/III期临床试验和雾化吸入用FB2001拟治疗轻型、普通型新冠病毒感染患者的II/III期临床试验。截至2022年12月31日,注射用FB2001的国际多中心、随机、双盲、安慰剂对照II/III期临床试验已获得中国、澳大利亚、菲律宾等多个国家的研究批准,受试者已入组并给药。
广生堂GST-HG171
广生堂开发的口服小分子广谱抗新型冠状病毒3CL蛋白酶抑制剂1类创新药GST-HG171(泰阿特韦)联合利托那韦(合称“泰中定”)临床试验(IIT)结果显示泰中定具有优越的抗新冠病毒疗效,新冠患者核酸转阴时间明显优于阳性对照Paxlovid及安慰剂对照,同时安全性和耐受性良好,达到试验预期目的。广生堂已全面启动泰中定的II/III期关键性注册临床研究,目前正在全国30余家中心招募受试者。
开拓药业普克鲁胺
开拓药业去年4月曾披露其在研新冠口服药普克鲁胺治疗轻中症非住院新冠患者III期临床试验的关键数据,但此后一直没有更新消息。而该药也因雄激素受体的作用机理一直受到业内质疑。
此外,盐野义的新型3CL蛋白酶抑制剂、新冠口服药Ensitrelvir(恩斯特韦)也在今年1月向国家药监局正式递交了上市申请。中国生物制药有限公司披露旗下正大天晴药业集团有限公司与盐野义有限公司签订新型冠状病毒感染治疗药物Ensitrelvir中国大陆地区的推广协议,合作期限为5年。
结语
目前,防治传染病仍以预防为主。笔者认为相对感染后服用有副作用的抗病毒药物而言,提前接种疫苗是风险收益比更高的选择。但过去的经验告诉我们,面对疫情,合理备药也很有必要。
那么下一个问题如何合理备药?
先声的先诺欣,广生堂的泰中定和辉瑞药物类似都是复方制剂,由3CL蛋白酶抑制剂和低剂量CYP抑制剂组成。
先诺欣为口服小分子新冠病毒治疗药物,用于治疗成人伴有进展为重症高风险因素的轻至中度新冠患者,例如伴有高龄、慢性肾脏疾病、糖尿病、心血管疾病、慢性肺病等重症高风险因素的患者。
患者应在医师指导下严格按说明书用药,使用中应高度关注说明书中列明的与其他药物相互作用信息。据报道禁止与辉瑞P药合用的药物共有28种,所以一定要严格按照医嘱服用,不建议擅自服用。