经典名方大爆发
来源:药智数据 | 发布时间:2026-04-30
摘要:2026年第一季度,中药注册申报以补充申请(754个品种)为核心,这主要是企业为满足即将施行的《中药注册管理专门规定》的合规要求,旨在完善药品安全信息并避免批文失效。与此同时,经典名方复方制剂(3.1类)的研发与上市转化加速,本季度共有8个经典名方颗粒产品获批上市,成为行业亮点。
01注册与受理
01
申报情况概览2026年第一季度CDE共受理新的中药注册申请1141个品种(受理号1222个),同比上升105%。申报类型以补充申请为主,数量高达754个品种,接下来为IND 31个品种、NDA 16个品种,ANDA只有1个品种,为河南蓝天药业有限公司和黄山精制药业有限公司联合申报的热淋清颗粒,2020版中药注册新规实行5年,通过同名同方ANDA的药品仅一个,各企业对于同名同方药的研发逐渐趋于保守。
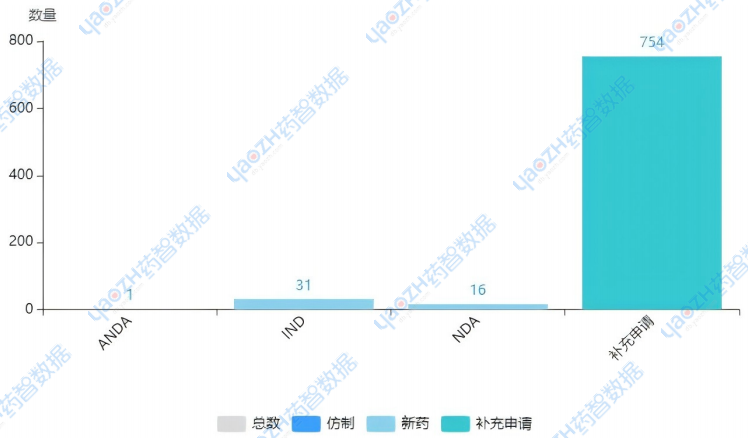
图1 2026年第一季度CDE受理中药申报任务类型
除去补充申请、一次进口和仿制药来看,新药申报品种有47个,以1.1类新药为主,申报品种有24个,以IND为主申报,申报NDA的两个中药新药分别为双鱼颗粒(江苏康缘药业股份有限公司)和金柴胶囊(神威药业集团有限公司),两个新药的NDA均处于在审评审批中;紧随其后的是3.1类经典名方,申报品种有13个。
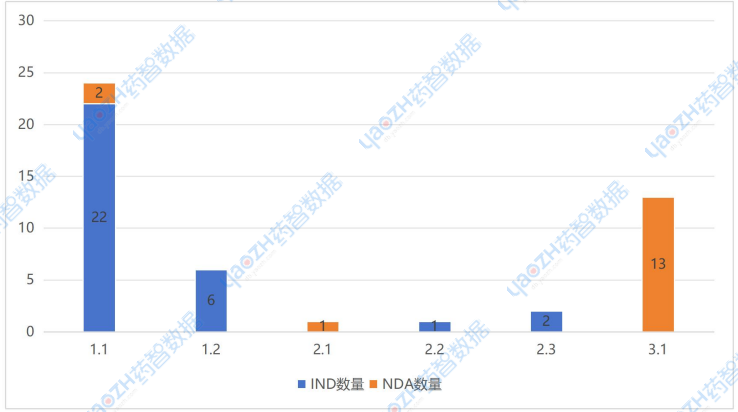
图2 2026年第一季度CDE受理中药新药注册分类品种数
02
审批情况概览2026年第一季度中,获得批准补充的中药品种最多。成为本季度的绝对主体。这一现象与 2026 年即将落地的《中药注册管理专门规定》“生死条款” 直接相关,大量企业集中提交说明书修订、工艺变更等补充申请,以完善品种安全性信息、满足再注册的合规要求,避免批文失效。
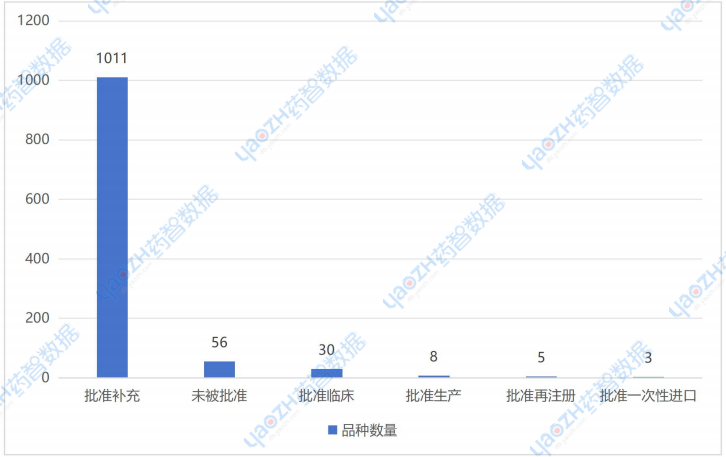
图3 2026年第一季度获得审批结论品种数
从已有注册分类品种的审批结论分析可以得出:
- 1.1类(中药复方创新药)共获批临床批件20件,中药创新药的研发管线储备充足,企业在源头创新上的投入仍在持续,但项目均处于临床阶段,距离商业化上市还有较长周期。
- 中药2类改良型新药整体申报数量有限,涵盖2.1、2.2、2.3、2.4多个细分类型,合计临床获批8件、仅2.1类出现1件未批准情况,且暂无生产获批项目,整体均处于研发早期阶段;其中2.3类增加功能主治申报数量最多,成为改良主流方向。
- 3.1类经典名方复方制剂获批生产批件8件,同时有4件申请未获批准,未批准率约33%。经典名方的上市转化进程正在加速。
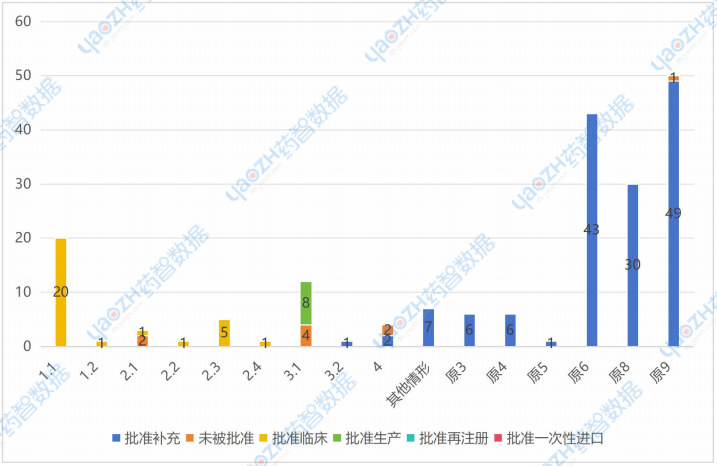
图4 2026年第一季度各注册类型审批结论
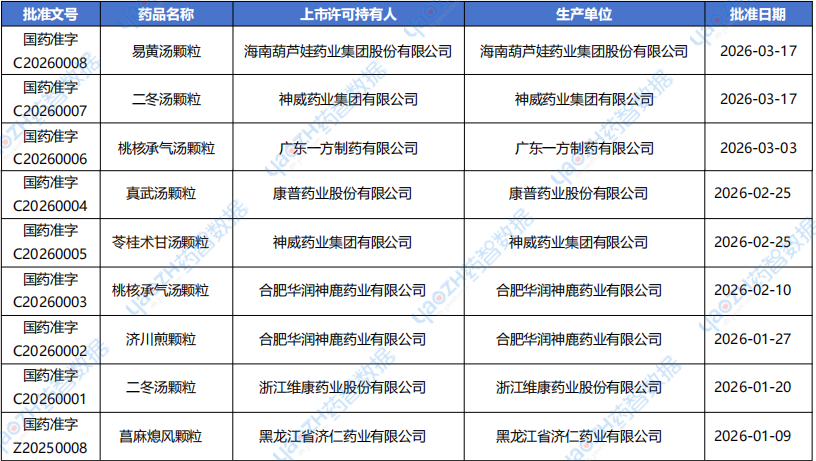
下表为2026年第一季度获批上市品种,其中黑龙江省济仁药业有限公司的菖麻熄风颗粒于2025年11月签发生产批件,但官方批准日期为2026年1月9日。表1 2026年第一季度获批上市的中药
02临床试验情况
2026年第一季度,CDE与中国临床试验注册中心登记的重要的中药相关药物临床试验共计60个,其中CDE公示登记的中药相关药物临床试验共计27个,同比下降6.9%。临床试验登记数量小幅回落,整体呈现持续走低的态势,主要受中药三结合政策全面实施影响,带动中药临床试验登记数量稳步下行。干预性研究占比高达 50%,安全性和有效性研究占比 35%,二者合计占比 85%,是当前中药临床试验的绝对主体。
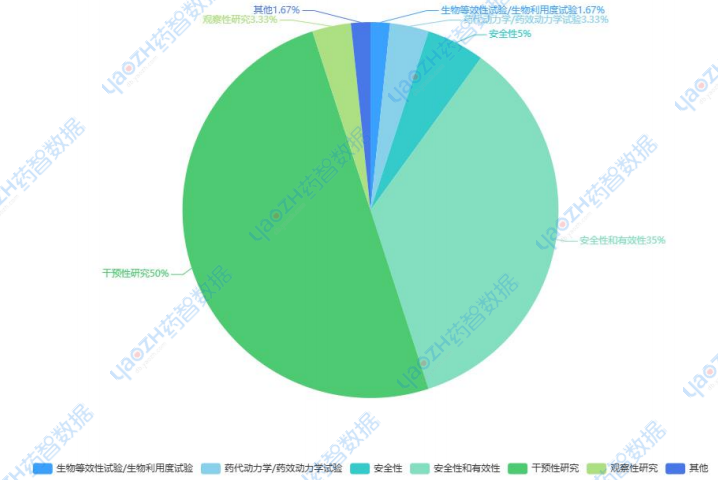
图5 2026年第一季度中药临床试验类型
03结语
2026年第一季度中药研发格局呈现鲜明的 “合规优先、存量挖潜、创新蓄力” 特征:补充申请占比大为行业合规刚需,经典名方批量上市成为核心亮点,创新与改良研发仍处早期蓄力阶段,临床试验聚焦高质量确证性研究。