吸入式疫苗已来,mRNA新冠疫苗还要多久
来源:药智网 | 发布时间:2022-11-09
摘要:吸入用疫苗相较于肌肉注射,吸入方式能多刺激一种免疫反应,即黏膜免疫。此前,世界卫生组织也对黏膜免疫的免疫方式进行了推荐,认为开发诱导黏膜免疫的疫苗是未来的方向。
自10月26日上海正式启动吸入式新冠疫苗加强针接种以来,康希诺的股价就如过山车般刺激,时而出现63.38%的暴涨,时而又出现34.75%的暴跌。
在暴涨和暴跌中展现了人们压抑和暴躁的情绪的极端化表达:失去耐心又隐隐期盼着这款新型新冠疫苗能够结束这场旷日持久的新冠疫情。
事实上,在新冠疫苗这条赛道上,各种技术路线下的产品基本都已闪亮登场。步入后疫情时代,随着全球新冠疫苗接种增速放缓,第一梯队的参赛者多数已经进入滑坡阶段,而未能赶上步伐的参赛者们,当时代的车轮无情地碾过之后,还能剩下什么?
能否再续辉煌?
康希诺的这款吸入式新冠疫苗之所以备受关注,主要在于其特殊的接种方式。
相较于肌肉注射,吸入方式能多刺激一种免疫反应,即黏膜免疫。此前,世界卫生组织也对黏膜免疫的免疫方式进行了推荐,认为开发诱导黏膜免疫的疫苗是未来的方向。
吸入用疫苗在有效提高体液中和抗体水平的同时,还可以在呼吸道的黏膜中产生抗体IgA,可以弥补现阶段疫苗无法阻止奥密克戎感染上呼吸道的短板。
康希诺的腺病毒载体新冠疫苗之所以能够最先成为吸入用疫苗,还与它自主研发的特点相关:一方面由于其选用腺病毒载体,可以在肺部有效进入靶细胞,表达目标抗原;另一方面由于其药学特性,使得这个疫苗配方可以在筛网震动雾化器中实现气雾化,并不降低疫苗的活性。
目前使用的灭活疫苗需使用铝佐剂,因此无法通过气雾化设备形成合适大小的微粒,而mRNA的结构相对脆弱,在雾化过程中容易失活,因此短期内无法改为吸入用。
这款吸入式新冠疫苗于9月4日经国家药监局组织论证同意作为加强针纳入紧急使用。在此前康希诺透露的消息中显示,相较于肌注疫苗里十分常见的不良反应,如头疼、疲乏和发热,在吸入疫苗里发生总量大幅下降,在老年人中下降幅度更大,其中三级的不良反应,如发热已经下降到百分之零点几;使用吸入用新冠疫苗序贯加强后28天,针对Omicron活病毒的交叉中和抗体滴度是用灭活疫苗同源加强的22.8倍。
这给了市场足够的想象力,那么,吸入式新冠疫苗是否会让康希诺的业绩再创辉煌?
此前,康希诺靠着新冠疫苗“克威莎”的红利,顺利实现扭亏。2021年,康希诺生物实现营收43亿元,实现净利润约19.14亿元,账上现金也达到创纪录的75亿元。
不过,从2022年开始,康希诺的业绩出现大幅下滑。
根据刚刚公布的三季度报,康希诺今年前三季度总营收为7.07亿元,同比下降77.08%;净利润-4.74亿元,同比下降135.57%;归母扣非净利润约为-5.83亿元,同比下降145.7%。主要为新冠疫苗需求量较去年同期大幅下降,产品价格调整,及对存在减值迹象的存货计提跌价准备所致。
11月1日,康希诺发布消息称,继上海之后,江苏省十三个城市也已开展吸入用新冠疫苗的部署工作。其中,无锡市共设9个吸入用新冠疫苗接种点,11月中旬开始可在门诊进行接种,淮安市有18个接种点;11月4日,康希诺董事长宇学峰在2022亚布力论坛创新年会上表示,康希诺经口吸入的新冠疫苗最近在全国各地开始全面铺开使用。
作为国内首款,康希诺的这款吸入式新冠疫苗确实有成为“爆款”的潜质,甚至可能成为新冠疫苗的“终结者”。如此一来,那些还处在研发阶段的新冠疫苗会不会前景堪忧?
mRNA新冠疫苗还要多久?
11月4日,德国总理在中德两国总理联合记者会上宣布,由德国企业BioNTech研发的mRNA新冠疫苗,将可在中国为在华生活的外国人接种。朔尔茨说,这只是“第一步”,他期待未来该疫苗的在华受惠者范围能够进一步扩大。
的确,这款由复星医药通过支付8500万美元许可费与35%的毛利销售提成等合作条款引进的mRNA新冠疫苗“复必泰”在中国的上市之路实在太过曲折。2020年12月,复必泰就启动了Ⅱ期临床试验,试验共入组950人,主要研究疫苗在中国大陆健康人群中的安全性,原计划于2021年12月结束,后延期至2022年4月,之后再度延期至10月。
如今德国总理访华,为复必泰在中国获批作出了“一小步”贡献,也让这款明星产品重回市场焦点。辉瑞正是凭借此款疫苗产品在2021年度实现了高达367.8亿美元的总营收,重新夺回全球制药Top1的宝座;复必泰在过去虽然只有在港澳台地区获批上市,就已经成为复星医药三大超10亿营收的龙头产品。
而在复必泰蛰伏的这段时间里,我们看到国内一众疫苗企业正在紧锣密鼓地快速推进国产mRNA新冠疫苗的进程。
据统计,国内聚焦mRNA药物研发的创新企业有十余家,主要有艾博生物、丽凡达生物、蓝鹊生物、斯微生物等;布局了mRNA新冠疫苗的企业包括沃森生物、艾美疫苗、斯微生物、康希诺等。
其中,沃森生物进度最快。
11月3日,沃森生物公告称,与复旦大学、蓝鹊生物共同研发的“新型冠状病毒变异株mRNA疫苗(S蛋白嵌合体)”已于近日获得Ⅲb期临床试验的《伦理审查批件》。
而就在9月,沃森生物另外一款与艾博生物共同研发的mRNA新冠疫苗已获得印度尼西亚国家食品药品监管局批准的紧急使用授权(EUA)。
艾美疫苗没有吃到上一轮新冠疫苗的红利,想必有些心急,于是于2021年5月,斥资10.42亿元获得丽凡达生物50.1546%的股权,其中部分以现金款项1.85亿元结算、部分以向丽凡达生物相关股东发行股份的方式结算。
丽凡达生物是mRNA技术赛道上的明星企业,其聚焦传染病疫苗、肿瘤、罕见病及其他蛋白缺陷类疾病的mRNA药物和mRNA美容抗衰等创新型产品。2021年3月,丽凡达生物研发的mRNA新冠疫苗获临床试验批准,成为我国第三个获批临床试验的mRNA新冠疫苗,目前正在中国进行II期临床,并已于2022年6月启动了全球III期临床。
斯微生物自主研发的mRNA新冠疫苗(SW-BIC-213)Ⅲ期临床试验已于2022年10月16日在老挝正式启动,该研究为随机、对照、双盲设定,评估作为序贯加强接种对于18岁及以上健康人群的免疫原性和安全性。斯微生物是中国首家在海外开展新冠迭代mRNA疫苗Ⅲ期临床的企业。根据老挝Ⅰ期和Ⅱ期临床观察显示,SW-BIC-213安全性良好,无严重不良事件和特别关注的不良事件,接种2针后14天,25ug低剂量组和45ug高剂量组对于Omicron中和抗体滴度分别为康复患者血清的2.0倍和3.3倍。此外,斯微生物已经获得巴西的临床I期、II期、III期的批件。
石药集团于2022年8月曾发布公告称其针对新型冠状病毒变异毒株自主研发的mRNA疫苗,目前已开展了6项临床研究,其中已完成一项序贯加强免疫的临床研究,其安全性和免疫原性均达到预期,目前已开始II期临床研究。
康希诺的mRNA新冠疫苗的研发按计划推进,目前处于II期临床阶段,成人组已完成入组;并已启动“3+1”序贯临床试验。同时,康希诺正在建设mRNA生产基地,一期项目设计产能1亿剂,预计在今年年底进行验证调试。
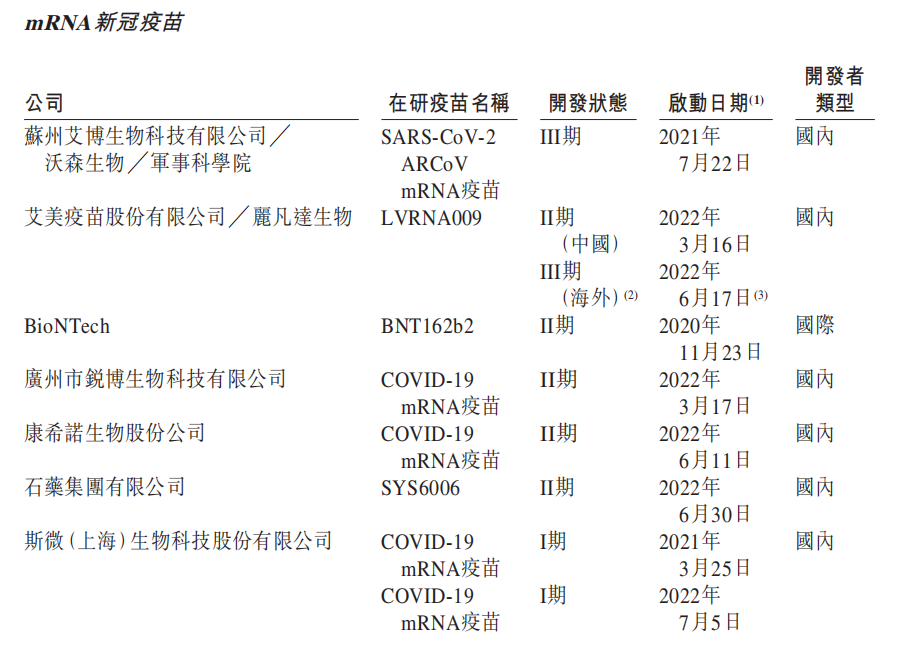
国内mRNA新冠疫苗在研情况
来源:艾美疫苗招股书
如此庞大的投入,也预示着mRNA新冠疫苗在国内的获批已势不可挡。
不过根据最新新冠疫苗接种数据,截至2022年11月4日,31个省(自治区、直辖市)和新疆生产建设兵团累计报告接种新冠病毒疫苗34.40亿剂次。国内基础免疫已在2021年基本完成,从今年开始,国内新冠疫苗市场仅剩加强针市场。随着新冠病毒的毒性逐渐减弱,对于新冠疫苗需求的紧迫性已经没那么高了。加强针市场具有一定的市场机会,远没有基础免疫的市场大。
在有限的市场需求下,如此庞大的mRNA新冠疫苗研究投入,今后该如何回收,这是摆在这些疫苗企业面前的另一个严峻问题。
结语
目前世界各地无症状感染的比例非常高,通过感染的方式或靠单一的疫苗形成群体免疫,是非常具有挑战性的,在保持抗体持续时间以及应对变异株方面,吸入式疫苗具有很强的便捷性优势。
而国内疫苗企业对mRNA疫苗的热情,纷纷加快mRNA研发平台技术进度的动作,可能野心不止于新冠疫苗,后续有望作为治疗性疫苗用于抗肿瘤疫苗、蛋白替代疗法、细胞疗法等。
病毒仍在变异,防疫政策也在随着变化,一切都还未尘埃落定。后续发展如何,我们还将持续关注。